 打印
打印
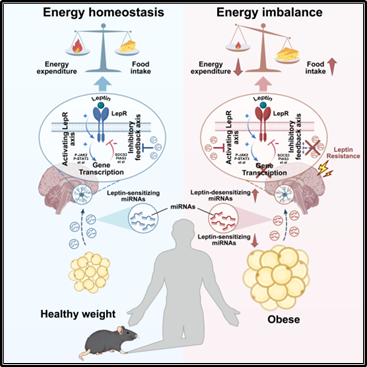
图 脂肪外泌体调控中枢瘦素敏感性维持能量稳态的模式图
在国家自然科学基金项目(批准号:82450002、82030026、82470865)等资助下,南京大学医学院附属鼓楼医院毕艳教授团队与南京大学生命科学学院李靓教授团队合作,在脂肪-大脑间通讯调控瘦素敏感性及能量稳态的机制研究方面取得进展。研究成果以“脂肪细胞外囊泡是中枢瘦素敏感性与能量稳态的关键调控因子(Adipocyte-Derived Extracellular Vesicles Are Key Regulators of Central Leptin Sensitivity and Energy Homeostasis)”为题,于2025年11月12日在《细胞·代谢》(Cell Metabolism)杂志在线发表。论文链接:https://doi.org/10.1016/j.cmet.2025.10.005。
肥胖与2型糖尿病、高血压等簇集共存,构成复杂疾病网络并加重医疗负担。生活方式干预、药物及代谢手术虽可短期减重,但疗效有限且易反弹,瓶颈在于肥胖病因机制尚未完全阐明。机体能量稳态由中枢-外周互作机制调控,其中脂-脑轴是维持长期能量稳态的关键反馈系统。瘦素是脂肪分泌、维持长期能量稳态的核心负反馈信号,其作用于中枢瘦素受体(Leptin receptor,LepR)神经元,抑制摄食并促进能量消耗。然而,肥胖常伴瘦素抵抗,阻碍外周能量储存信号向中枢有效传递。尽管针对瘦素抵抗机制研究已近三十年,但传统视角主要聚焦中枢内事件,未能从系统层面揭示其起始机制。
研究团队利用细胞外囊泡(Extracellular Vesicles,EVs)示踪平台,结合病毒介导的基因编辑技术和多种转基因小鼠,发现脂肪EVs及其微小RNA(MicroRNAs,miRNAs)是调控中枢瘦素敏感性和维持能量稳态的关键因子。研究团队通过小RNA测序和人工智能靶点分析,对脂肪EV miRNA 功能特征进行分类:一类为瘦素增敏型,通过抑制LepR信号负反馈因子增强信号;一类为瘦素去敏型,通过抑制LepR信号下游效应分子减弱信号。健康状态下脂肪EV富含瘦素增敏型miRNA,其缺失是瘦素抵抗及肥胖的关键驱动因素。该研究阐明了脂肪EVs的脑靶向机制,构建高效脑靶向工程化外泌体,实现向中枢精准递送瘦素增敏型miRNAs,能显著恢复中枢瘦素敏感性,促进减重并实现代谢重建(图)。
该研究从系统角度阐明脂-脑通讯异常是驱动中枢瘦素抵抗的核心机制,证实脂肪EVs及其miRNAs是调控中枢瘦素敏感性的关键分子。该研究推动瘦素抵抗研究范式由传统“以大脑为中心”转向“器官间通信”,为解决中枢瘦素抵抗及肥胖治疗开辟潜在全新策略。
