 打印
打印
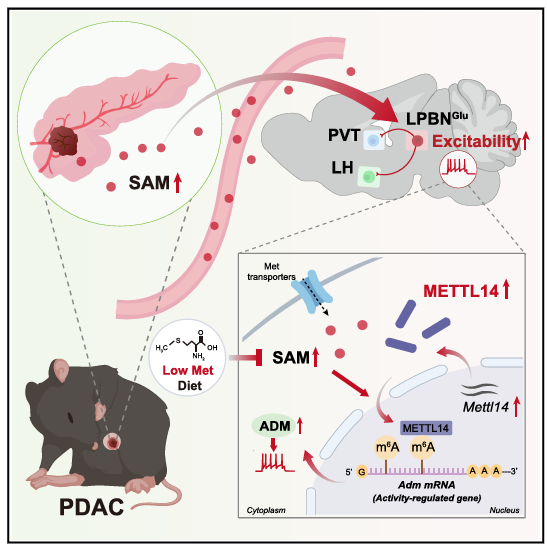
图 METTL14介导肿瘤–神经互作驱动胰腺癌疼痛–抑郁共病
在国家自然科学基金项目(批准号:82471238、824B2028)等资助下,中山大学谢敬敦教授团队在胰腺癌肿瘤–神经互作机制研究方面取得进展。研究成果以“METTL14整合肿瘤衍生SAM驱动胰腺癌臂旁核表观遗传重构(METTL14 Integrates Tumor-Derived SAM to Drive Parabrachial Epigenetic Rewiring in Pancreatic Cancer)”为题,于2025年11月4日在《神经元》(Neuron)杂志上在线发表。全文链接:https://www.sciencedirect.com/science/article/abs/pii/S089662732500755X。
疼痛是影响肿瘤患者生活质量的最常见且最显著症状之一。在胰腺导管腺癌(pancreatic ductal adenocarcinoma,PDAC)患者中,约 90% 经历难以控制的持续性疼痛,且常伴发抑郁等精神共病,这种情况不仅降低治疗耐受性,还严重影响生存预后。然而,外周肿瘤如何通过影响中枢神经系统重塑从而驱动疼痛–抑郁共病的机制尚未明确。
研究团队通过构建小鼠PDAC模型,结合多组学分析、神经示踪、光遗传及化学遗传学技术,发现外侧臂旁核谷氨酸能神经元(LPBNGlu)中甲基转移酶样14(methyltransferase-like 14,METTL14)显著上调,而且是驱动PDAC相关疼痛–抑郁共病的关键调控因子。METTL14通过协同肿瘤衍生的S-腺苷甲硫氨酸(S-adenosylmethionine,SAM),促进肾上腺髓质素(adrenomedullin,ADM)mRNA的N6-甲基腺苷(m6A)修饰,从而诱导神经元过度兴奋,增强LPBNGlu–室旁丘脑(PVTGlu)和外侧下丘脑(LHGlu)的环路投射,最终导致共病的发生。进一步研究发现,PDAC患者和模型小鼠的循环SAM水平均显著升高,并与临床疼痛及抑郁症状严重程度密切相关。通过蛋氨酸限制饮食降低体内SAM水平,可有效减轻神经元过度兴奋,缓解共病症状,并同时抑制肿瘤生长,获得镇痛-抗癌协同的效果(图)。
该研究明确了肿瘤–神经互作在胰腺癌疼痛-抑郁共病形成中的关键作用,揭示了SAM–METTL14–ADM信号通路及LPBNGlu–PVTGlu / LHGlu神经环路介导脑功能重塑的新机制,为胰腺癌共病行为的代谢干预提供了潜在治疗靶点。
