 打印
打印
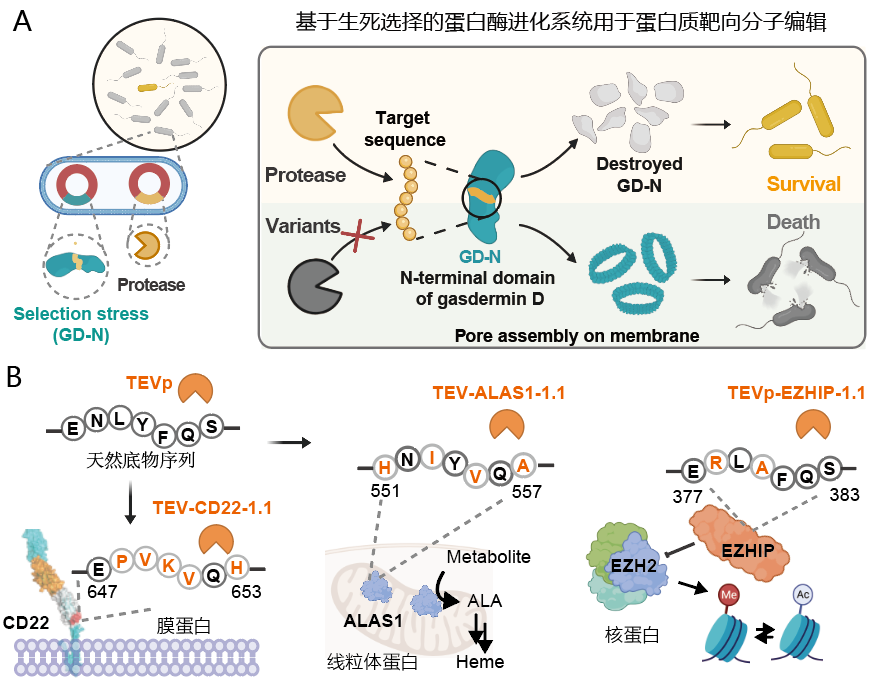
图 基于生死选择的蛋白质酶进化系统
在国家自然科学基金项目(批准号:22077059、22277048、22477053、92253304、 21937001、22137001、91753000)等资助下,南方科技大学化学系王杰团队联合北京大学陈鹏团队,在蛋白质靶向编辑领域取得进展。相关成果以“基于gasdermin的生死筛选进化系统用于蛋白酶特异性的重塑(A gasdermin-based life–death evolution system for reprogramming protease specificity)”为题,于2025年10月31日在《自然・化学生物学》(Nature Chemical Biology)期刊上发表,论文链接:https://www.nature.com/articles/s41589-025-02063-3。
分子的精准编辑与高效转化是化学领域的核心科学问题。目前,随着新型金属催化剂、配体及光催化反应体系的持续开发,复杂有机小分子的编辑已取得明显进展,但DNA、蛋白质等生物大分子的精准编辑仍面临巨大挑战。
基因编辑通过可编程的RNA与Cas蛋白实现了DNA的精准修改。借鉴这一理念,若能以类似方式重塑蛋白酶的底物特异性,使其识别并切割特定蛋白靶点,将为蛋白质层面精准编辑开辟新途径。与基因编辑需识别15~18个碱基不同,蛋白酶仅需识别5~7个氨基酸即可在蛋白质组中实现特异性切割。因此,通过定向进化改造蛋白酶,有望开发出可编程的蛋白质编辑工具,实现蛋白质功能层面的精准干预。
针对蛋白质靶向编辑的机遇与挑战,上述团队开发了基于Gasdermin D(GSDMD)的“生死选择”型蛋白酶定向进化平台。该平台利用GSDMD N端结构域(GD-N)在大肠杆菌中表达可抑制生长的特性,将其作为筛选标签。在GD-N的loop区插入目标蛋白酶识别序列,构建筛选系统:若蛋白酶突变体可切割该序列,GD-N即失活,细胞存活;反之细胞生长受抑制。经连续培养,高活性突变体可被快速富集,单轮筛选即可实现百万倍富集效率。
利用该平台,团队成功对TEV蛋白酶进行定向进化,获得可特异性识别并切割CD22(B细胞受体)、ALAS1(血红素合成关键酶),EZHIP(调控H3K27甲基化的核蛋白)等多种内源性蛋白的突变体。由此表明,该GSDMD平台具备高效率、高覆盖度等优势,可以为蛋白酶特异性重编程及内源性蛋白精准切割提供通用工具。
