 打印
打印
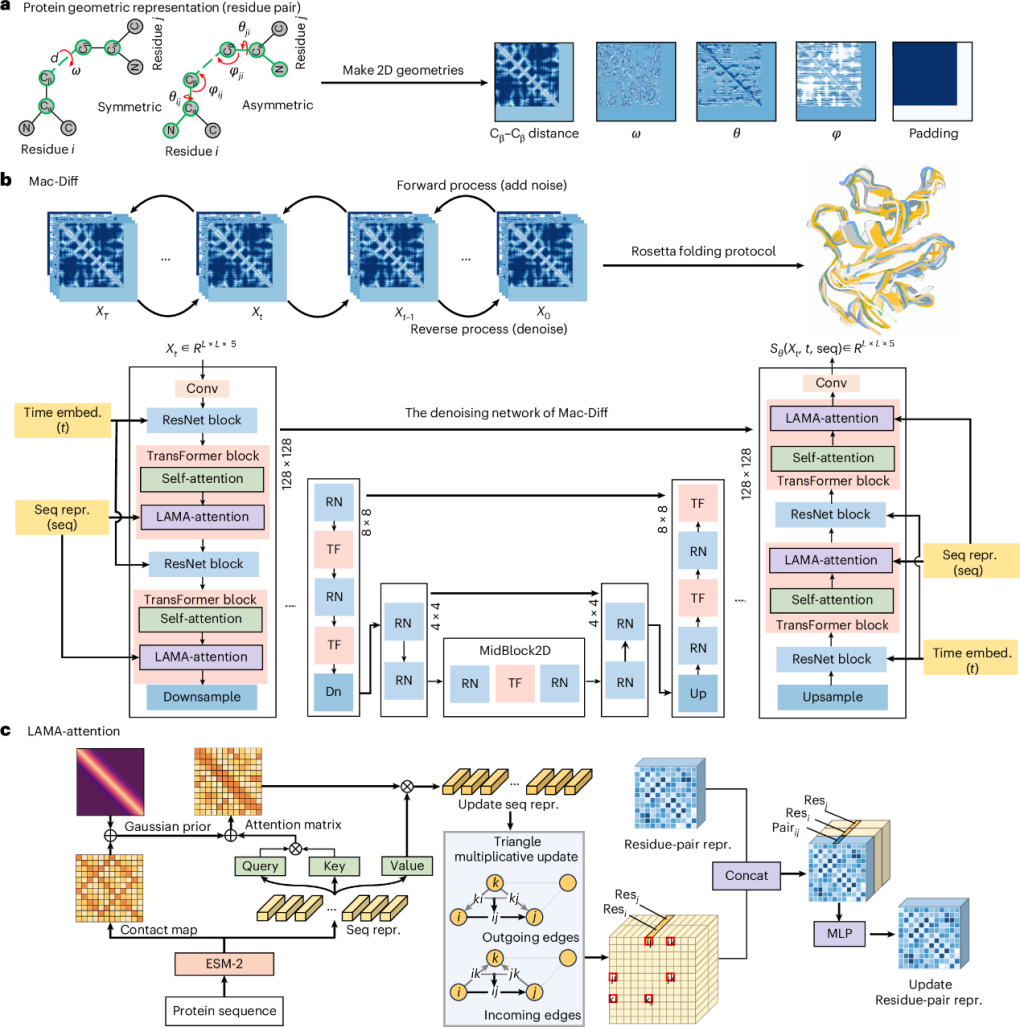
图 Mac-Diff架构概述
在国家自然科学基金项目(批准号:82425104、62276099)等资助下,华东师范大学/华东理工大学李洪林教授团队,联合华东师范大学计算机学院张凯教授团队和复旦大学类脑智能科学与技术研究院张捷研究员团队等多家单位,在基于AI生成预测蛋白质构象系综方面取得进展。研究成果以“一种基于局部感知模态对齐的条件扩散方法用于生成多样化的蛋白质构象系综(Conditional diffusion with locality-aware modal alignment for generating diverse protein conformational ensembles)” 为题,于2026年2月25日在线发表于《自然•机器智能》(Nature Machine Intelligence)杂志。论文链接:https://www.nature.com/articles/s42256-026-01198-9
蛋白质构象系综的精准建模是理解分子功能机制与开展基于结构药物设计的关键前提。蛋白质在生理条件下并非停留于单一静态结构,而是在多重亚稳态之间动态转换,这种内禀灵活性直接决定其催化、识别与变构调控等生物学功能。然而,动态构象的获取仍面临多重挑战:传统结构生物学方法多聚焦于单一稳态构象,难以捕捉瞬态中间态;分子动力学模拟虽然能够采集连续的动力学轨迹,但受限于积分步长与实际生物事件的时间尺度,长时间、大尺度采样效率较低;近年来涌现的蛋白质结构预测模型虽然显著提升了静态结构的精度,但往往偏向热力学最低能态,对完整构象景观的覆盖能力不足;此外,对结构预测模型的序列表征和组件依赖可能导致预测结果偏向于单个主导结构。因此,如何充分利用序列中蕴含的进化信息与物理先验约束,高效生成真实且多样的蛋白质构象集合,成为当前亟待突破的核心科学问题。
针对上述瓶颈,研究团队提出了一种“模态对齐条件扩散”算法—Mac-Diff,实现蛋白质构象分布的快速生成与精准采样。该模型在扩散生成框架中引入局部感知的模态对齐注意力模块,将蛋白质语言模型的序列表征、残基对空间几何关系与物理先验深度融合,引导注意力聚焦真实存在相互作用的局部邻域,从而实现跨模态信息的精准对齐与高效传递;同时结合三角乘法更新机制与多尺度去噪网络,显式建模残基间几何依赖关系,并通过逐步去噪过程还原多样化的构象。该策略使模型在保持采样保真度-多样性的同时显著提升采样效率,并且在分布一致性、残基接触概率等多个指标上实现全面提升,为探索复杂的构象空间提供了新的生成式建模范式。模型在真实生物学场景下成功捕获多种蛋白质中与功能相关的开放态、闭合态及罕见中间态构象,展现出对蛋白质构象异质性的强刻画能力。
该项研究实现了人工智能、计算生物学与药学等专业的深度融合,不仅大幅降低了蛋白质动力学采样成本,加速分子模拟流程,也为解析变构调控机制及靶向瞬时构象的药物设计提供了高效可靠的新工具,展示了跨学科协同在推动蛋白质动态构象研究中的关键作用。
