 打印
打印
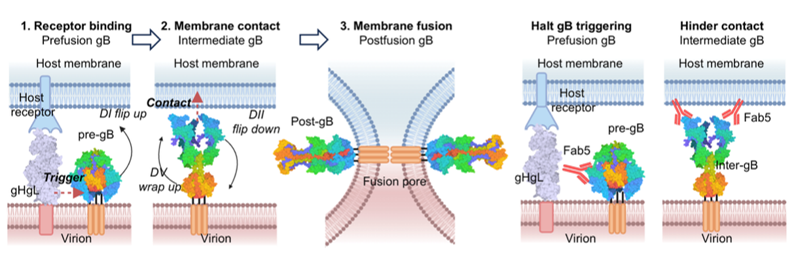
图 γ疱疹病毒gB介导膜融合机制及Fab5潜在中和机制
在国家自然科学基金项目(批准号:U24A20743、32441094、82402614)等资助下,中山大学肿瘤防治中心曾木圣研究员、孙聪副研究员团队联合南方科技大学刘铮研究员团队,在γ疱疹病毒广谱干预策略研究领域取得进展。研究成果以“一种针对伽马疱疹病毒gB的广谱保护抗体(A broadly protective antibody targeting gammaherpesvirus gB)”为题,于2026年2月2日在《自然》(Nature)杂志上发表。论文链接:https://www.nature.com/articles/s41586-026-10192-5。
γ疱疹病毒广泛感染人类及多种哺乳动物。其中,EB病毒(EBV)和卡波西肉瘤相关疱疹病毒(KSHV)是重要的人类致瘤病毒,与多种恶性肿瘤及自身免疫性疾病密切相关。由于不同属、不同宿主来源的病毒之间存在高度异质性,开发能够提供跨属、跨物种保护的广谱疫苗和中和抗体一直是该领域国际公认的难题。
作为包膜病毒,γ疱疹病毒感染宿主细胞依赖于高度保守的膜融合过程,γ疱疹病毒的感染依赖于高度保守的膜融合蛋白——糖蛋白B(gB)。研究团队基于前期研发的EBV嵌合纳米颗粒疫苗,通过抗原特异性单B细胞分选测序技术,成功筛选并鉴定出一株靶向gB的单克隆抗体Fab5;蛋白和细胞原位结合实验显示,Fab5能够高效结合EBV、rhLCV和MHV68等多种γ疱疹病毒gB,并有效阻断它们对细胞的感染(图);在小鼠、非人灵长类动物和人源化小鼠动物模型中研究发现,Fab5均能有效保护动物免于相应易感的γ疱疹病毒感染。研究进一步解析了Fab5与多种γ疱疹病毒gB的冷冻电镜结构,结果显示Fab5结合于gB的结构域I,该区域在不同γ疱疹病毒中整体构象高度保守;序列与结构映射表明,Fab5所识别的结构域I表位在γ疱疹病毒属间呈现功能保守、序列部分可变的特征,该结构域在gB的前融合与后融合构象中均保持较高的结构稳定性和表面可及性,构成了其保守的中和识别表位,提示Fab5可能通过阻断gB在膜融合过程中的关键构象转变,或干扰gHgL-gB信号传递途径,从而实现γ疱疹病毒广谱中和。
这项研究通过筛选获得了广谱的γ疱疹病毒中和抗体Fab5,并解析了其所识别的保守关键中和表位结构域I,为疱疹病毒相关肿瘤及自身免疫性疾病的广谱疫苗研发提供科学基础。