 打印
打印
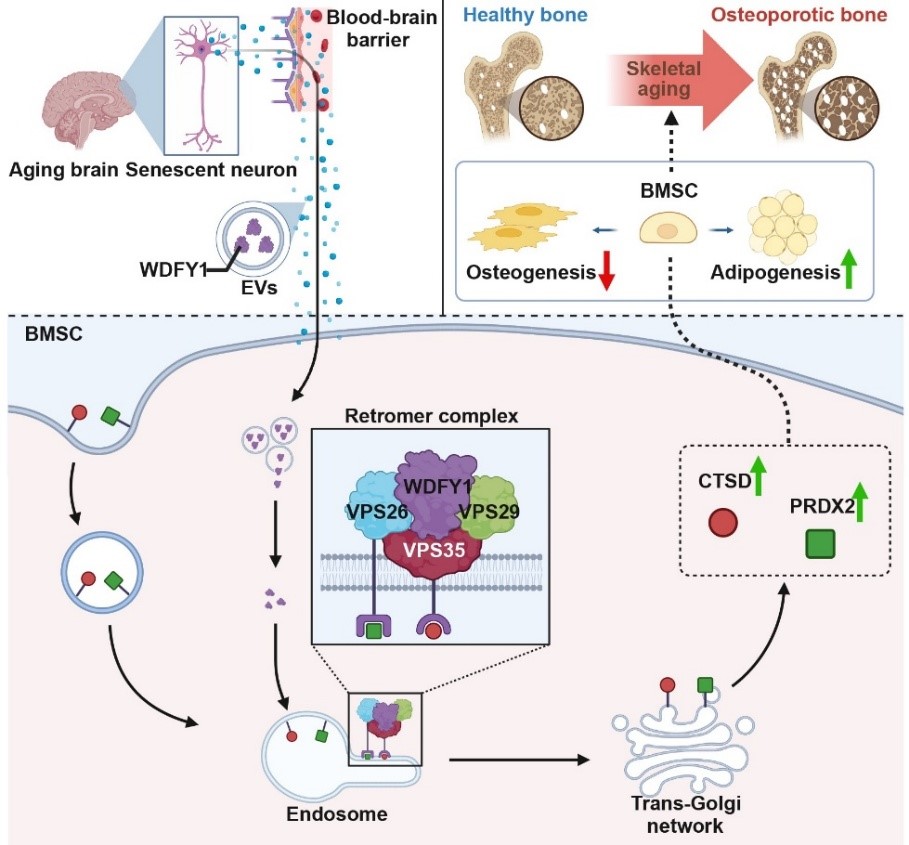
图 衰老大脑神经元细胞外囊泡通过转运WDFY1促骨质疏松发生的机制
在国家自然科学基金项目(批准号:82172501、82125023、82372479)等资助下,中南大学湘雅医院谢辉研究员、饶珊珊副研究员和陈春媛副研究员团队在大脑神经元衰老调控骨质疏松发生研究方面取得进展。相关研究成果以“大脑神经元来源WDFY1诱发骨量丢失(Brain neurons-derived WDFY1 induces bone loss)”为题,于2026年1月5日在线发表于《自然·衰老》(Nature Aging)杂志上。论文链接:https://doi.org/10.1038/s43587-025-01032-8
骨质疏松症是一种以骨量减少、骨微结构破坏为特征的全身性骨骼疾病,主要表现为疼痛、骨骼畸形和脆性骨折风险升高,严重影响老年人的生活质量。研究发现,多种脑源性因子参与骨骼的代谢调控过程。然而,衰老大脑是否影响骨骼代谢,促进骨质疏松发生,尚不清楚。
研究团队首先通过小鼠体内示踪发现,衰老大脑神经元释放的细胞外囊泡(extracellular vesicles,EVs)能够远程运输至骨组织,诱导骨质流失。进一步对EVs进行蛋白质组学分析表明,WD重复和FYVE结构域蛋白1(WD repeat and FYVE domain containing 1,WDFY1)在衰老大脑神经元来源的EVs中显著富集。单细胞核RNA测序和免疫荧光染色证实,WDFY1在衰老大脑的海马和大脑皮层神经元中高表达。利用转基因小鼠等动物模型对脑内Wdfy1基因调控后观察到,WDFY1蛋白可经由大脑神经元释放的EVs运输至骨组织,进而改变骨髓间充质干细胞分化方向,使其由成骨分化转向成脂分化,导致骨量下降。机制研究表明,WDFY1在骨髓间充质干细胞中通过结合内体表面的回收复合体VPS26A/B–VPS35–VPS29,促使组织蛋白酶D和过氧化物酶2向高尔基体回收,促进其向成脂分化。临床血浆样本检测显示,老年人群血浆及血浆来源的EVs中 WDFY1 水平显著高于年轻人群,且其表达水平与骨质疏松呈正相关,进一步表明WDFY1是骨质疏松发生的潜在致病因子。
该研究揭示了衰老大脑来源的细胞外囊泡富含 WDFY1,通过改变骨髓间充质干细胞分化命运调控骨质疏松发生的机制,为骨质疏松疾病的治疗提供了新思路。
