 打印
打印
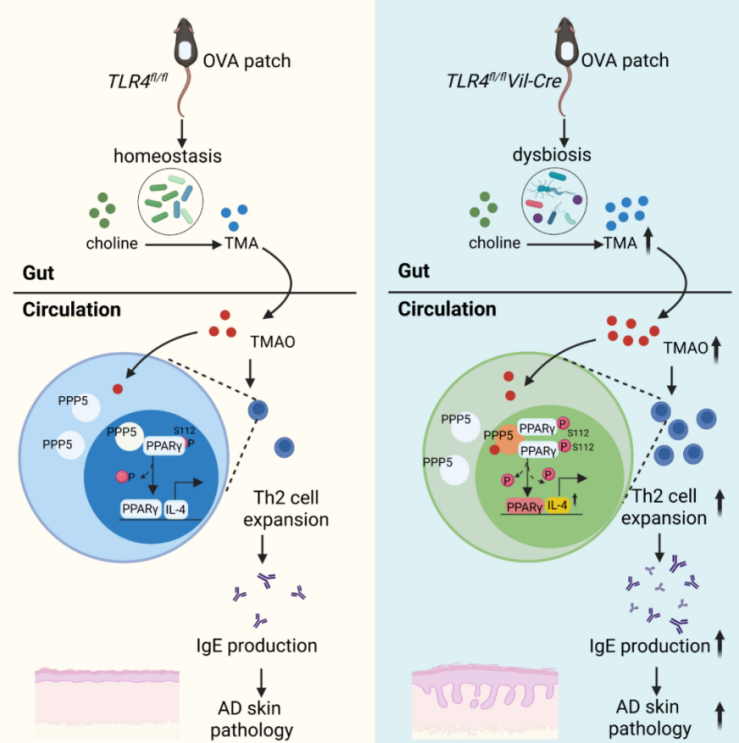
图 肠道菌群失调驱动Th2细胞分化加剧皮肤炎症的机制图
在国家自然科学基金项目(批准号:82271782)等资助下,南方医科大学左大明教授团队联合马骊教授、孙乐栋教授团队,在肠-皮轴调控特应性皮炎机制研究方面取得进展。相关研究成果以“肠道菌群失调通过微生物代谢物驱动的Th2细胞分化加剧皮肤炎症(Intestinal dysbiosis exacerbates skin inflammation via microbial metabolite-driven Th2 cell differentiation)”为题,于2026年4月16日在线发表于《免疫》(Immunity)杂志。论文链接:https://www.cell.com/immunity/fulltext/S1074-7613(26)00130-5。
特应性皮炎(AD)是一种复杂的慢性炎症性皮肤病。近年来,“肠-皮轴”在远端皮肤炎症中的系统性调控作用倍受关注,但其跨器官通讯的具体分子机制尚未阐明。
该团队研究发现,肠上皮细胞Toll样受体4(TLR4)缺失会引发显著的肠道菌群失调,表现为益生菌(如嗜黏蛋白阿克曼菌)丰度骤降,以及携带胆碱三甲胺裂解酶(CutC)的条件致病菌显著富集。这加速了肠道胆碱代谢,导致血液中氧化三甲胺(TMAO)水平异常升高。结合UK Biobank大型队列及临床AD患者数据,研究证实高膳食胆碱摄入与AD患病风险增加相关,且患者血浆TMAO水平与疾病严重程度呈显著正相关。进一步机制研究表明,TMAO能够直接结合并激活CD4⁺ T细胞内的蛋白磷酸酶5(PPP5),增强其对底物PPARγ的去磷酸化活性;去磷酸化的PPARγ进而启动Th2细胞分化相关的转录程序,从而诱发全身性Th2型免疫应答并加剧皮肤炎症。进一步干预实验显示,在CD4⁺ T细胞中特异性敲除PPARγ,或使用PPP家族抑制剂Fostriecin,均能有效阻断TMAO诱导的病理过程并显著缓解AD小鼠的皮肤炎症(图)。
该研究揭示了肠道天然免疫经“胆碱-TMAO-PPP5-PPARγ”调控Th2细胞分化的新机制,不仅深化了人们对“肠-皮轴”跨器官对话的理解,也为未来通过调节肠道微生态、膳食干预或靶向特定分子通路治疗AD等过敏性疾病提供了全新的转化干预策略。