 打印
打印

图1 我国学者创立了首个基于内质网相关降解(endoplasmic reticulum associated degradation,ERAD)途径的靶向蛋白降解技术。该技术利用小分子化合物,在pM-nM浓度下高效靶向降解跨膜蛋白,为神经退行性疾病及肿瘤等重大疾病的口服药物研发提供了新路径。图示为ERADEC作用机制的写意阐述:右侧山川建筑象征细胞,中央泼墨代表内质网,神奇画笔(ERAD)被靶向降解小分子(ERAD-engaging Chimera,ERADEC,即泼墨中的亮点)诱导,经由内质网相关降解途径选择性降解致病蛋白,从而实现抵御疾病(左侧船只)。
能否利用细胞具有的“自我清洁”能力,精准清除致病的跨膜蛋白,从而从根源上遏制疾病?这一愿景,如今正通过我国科学家的原创突破变为现实。在国家自然科学基金项目(批准号:82525103、82450901、82394422、82030105、82330109)等资助下,研究团队在靶向蛋白降解领域取得重大突破。他们设计出一类命名为 ERADEC的嵌合小分子化合物,通过“劫持”内质网泛素化连接酶,进而精准结合并降解导致疾病的膜蛋白—特别是以往药物难以清除的“顽固分子”。
这项研究一举攻克了两大长期存在的技术瓶颈:一是首次系统性地利用细胞自身的内质网相关降解系统(endoplasmic reticulum associated degradation,ERAD)机制来降解目标蛋白,使得位于细胞膜上的棘手靶点不再“无法清除”;二是绕过了传统药物必须依赖靶点上有特定“可成药结合口袋”的限制,拓展了可干预的疾病靶点范围。体现了我国在蛋白质稳态调控与靶向降解前沿领域的原创性突破,对神经退行性疾病、肿瘤等重大疾病的机制研究及新型口服药物研发具有重要意义。
亨廷顿病等神经退行性疾病的关键病理基础在于致病的突变蛋白在神经细胞中的持续积累。然而,这类蛋白通常缺乏可被传统药物“抓住”的结构位点,长期被视为“不可成药”靶标,干预手段十分有限。复旦大学生命科学学院鲁伯埙教授和海军军医大学盛春泉教授团队合作,借助细胞自身原有的“质量控制机制”—ERAD,实现了对细胞内在降解系统的“重定向”,识别并处理原本不会被降解的致病蛋白,从而实现对其水平的有效控制并抵御疾病(图1)。相关成果以“劫持内质网相关降解以靶向跨膜蛋白降解(Hijacking ER-associated degradation (ERAD) for targeted degradation of transmembrane proteins)”为题,于2026年3月19日在线发表于《细胞》(Cell)杂志。论文链接:https://www.cell.com/cell/abstract/S0092-8674(26)00105-4。
研究始于对一个小分子地奈德(desonide)的功能和作用机制解析。研究团队前期研究表明,desonide可抑制亨廷顿病关键致病蛋白(mutant huntingtin, mHTT)的毒性,但其具体机制尚不明确。为了揭示现象背后的科学机制,研究团队合作攻关,意外地发现小分子desonide并非简单地直接抑制mHTT功能,而是作为“分子桥梁”,通过结合细胞内的内质网定位E3泛素连接酶SYVN1,作为“分子胶”增强致病蛋白与SYVN1的结合,从而使致病蛋白被打上“降解(泛素化)”的标签并进入细胞降解系统(图2)。
基于上述机制研究,研究团队巧妙利用跨膜蛋白合成时会进入内质网进行折叠而难以接触到细胞质内降解系统这一特性,提出并建立了一种“劫持”ERAD的新技术策略—内质网相关降解招募型嵌合分子ERADEC降解体系。通过设计具有双重功能的小分子,一端识别目标蛋白,另一端连接内质网上的降解标签蛋白SYVN1,将目标蛋白主动“引入”ERAD通路,使其被选择性降解。与以往主要依赖细胞质降解系统的策略不同,这一方法利用内质网自身的降解机制用于跨膜蛋白靶向降解。
研究团队进一步以肿瘤免疫治疗中关键靶点PD-L1为模型进行验证,发现ERADEC在较低浓度(pM-nM量级)下即可实现对PD-L1的有效降解,证实了通过小分子化合物“劫持”ERAD这一经典的错误折叠蛋白降解机制,可以实现对跨膜蛋白的特异性降解,从而有效抑制肿瘤生长,其抗肿瘤效果优于临床广泛应用的PD-L1抗体阻断策略(图2)。与需要静脉注射的传统抗体药物相比,此类小分子降解剂具备可循环利用、有效用药浓度低及成本更低等优势,且有望推动肿瘤免疫治疗迈入口服给药的新阶段。该研究不仅提供了一种可行的技术方法,更提出了一种新的药物研发范式:相较于传统的蛋白功能抑制策略,直接诱导致病蛋白降解可能展现出更为显著的治疗潜力。
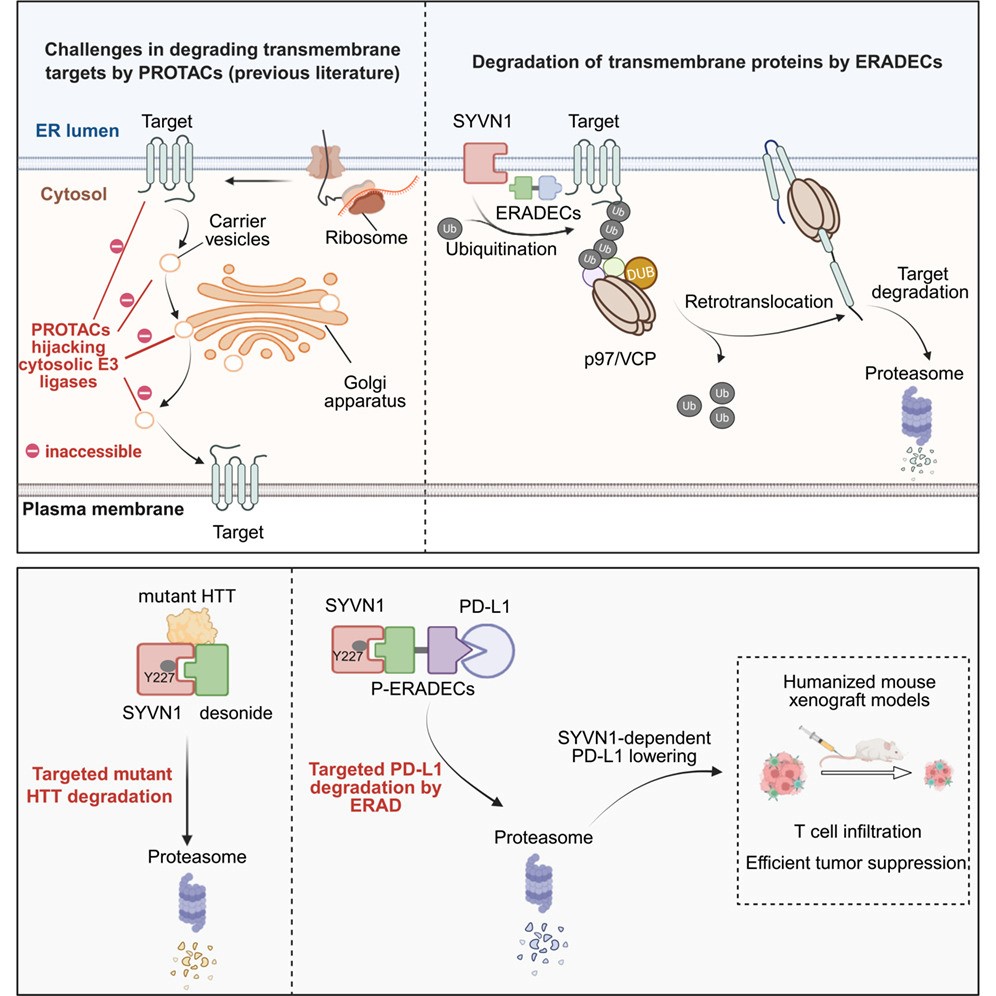
图2 靶向蛋白降解技术ERADEC的构建及干预应用
该研究成果的取得,得益于国家自然科学基金委员会青年科学基金项目(A类延续资助)、原创探索计划项目(延续资助)等长期、稳定的资助机制。同时,该成果亦是跨学科研究团队的深度协作,充分体现了聚力攻关与协同创新的科研模式优势。从最初现象发现到机制解析,再到技术体系的构建,整个研究过程彰显了基础研究在长期积累中不断孕育突破的特点。