 打印
打印
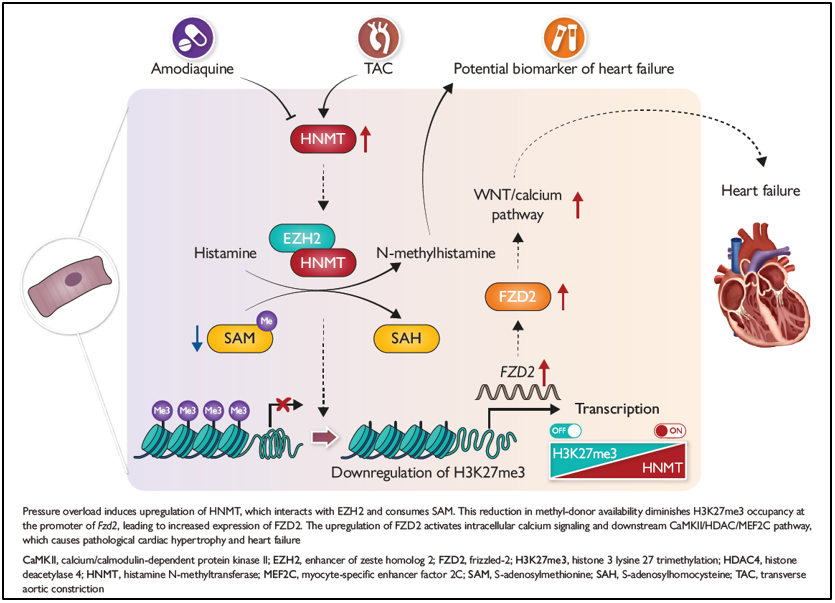
图 HNMT导致心力衰竭进展的机制
在国家自然科学基金项目(批准号:T2288101、82130010、82500458)等资助下,复旦大学附属中山医院葛均波院士、孙爱军教授团队与上海市徐汇区中心医院杨靖教授团队合作,在心力衰竭的代谢-表观遗传调控机制研究方面取得进展。研究成果以“组胺N-甲基转移酶上调介导心脏肥大与心力衰竭(Histamine N-methyltransferase upregulation, cardiac hypertrophy, and heart failure)”为题,于2026年1月23日在《欧洲心脏杂志》(European Heart Journal)上发表。论文链接:https://doi.org/10.1093/eurheartj/ehaf1065。
心力衰竭是多种心血管疾病的终末阶段,即便在现有规范治疗下,患者仍面临疾病进展与死亡的残余风险,亟需针对其病理生理机制探索新靶点。近年来研究发现,代谢中间产物可直接通过调控表观遗传修饰影响基因表达,这为理解心衰提供了新视角。然而,在衰竭的心脏中,是否存在特定的关键代谢物变化,通过“重写”表观遗传密码,从而导致心衰进展,这一科学问题尚未阐明。
该研究聚焦于心脏中清除组胺的关键代谢酶——组胺N-甲基转移酶(HNMT)。团队通过临床样本及动物模型证实,心力衰竭过程中心肌细胞HNMT表达显著上调。机制研究表明,上调的HNMT会消耗细胞内重要的甲基供体S-腺苷甲硫氨酸(SAM),并与组蛋白甲基转移酶EZH2结合,特异性降低WNT/CaMKII信号通路关键基因FZD2启动子区的抑制性组蛋白修饰H3K27me3水平,从而激活该信号通路,最终驱动心脏病理性肥厚与功能恶化。研究同时发现,心衰患者尿液中HNMT下游代谢物N-甲基组胺水平升高,提示其作为无创诊断标志物的潜力。尤为重要的是,应用已上市的抗疟药物阿莫地喹(HNMT抑制剂)干预心衰小鼠,可有效改善心功能,为“老药新用”提供了直接的临床前证据(图)。
该研究揭示了HNMT通过消耗SAM、扰动表观遗传修饰,进而激活特定信号通路的全新机制,阐明了代谢-表观遗传对话在心力衰竭中的关键作用,为心衰的生物标志物开发和治疗干预提供了新靶点与新策略。