 打印
打印
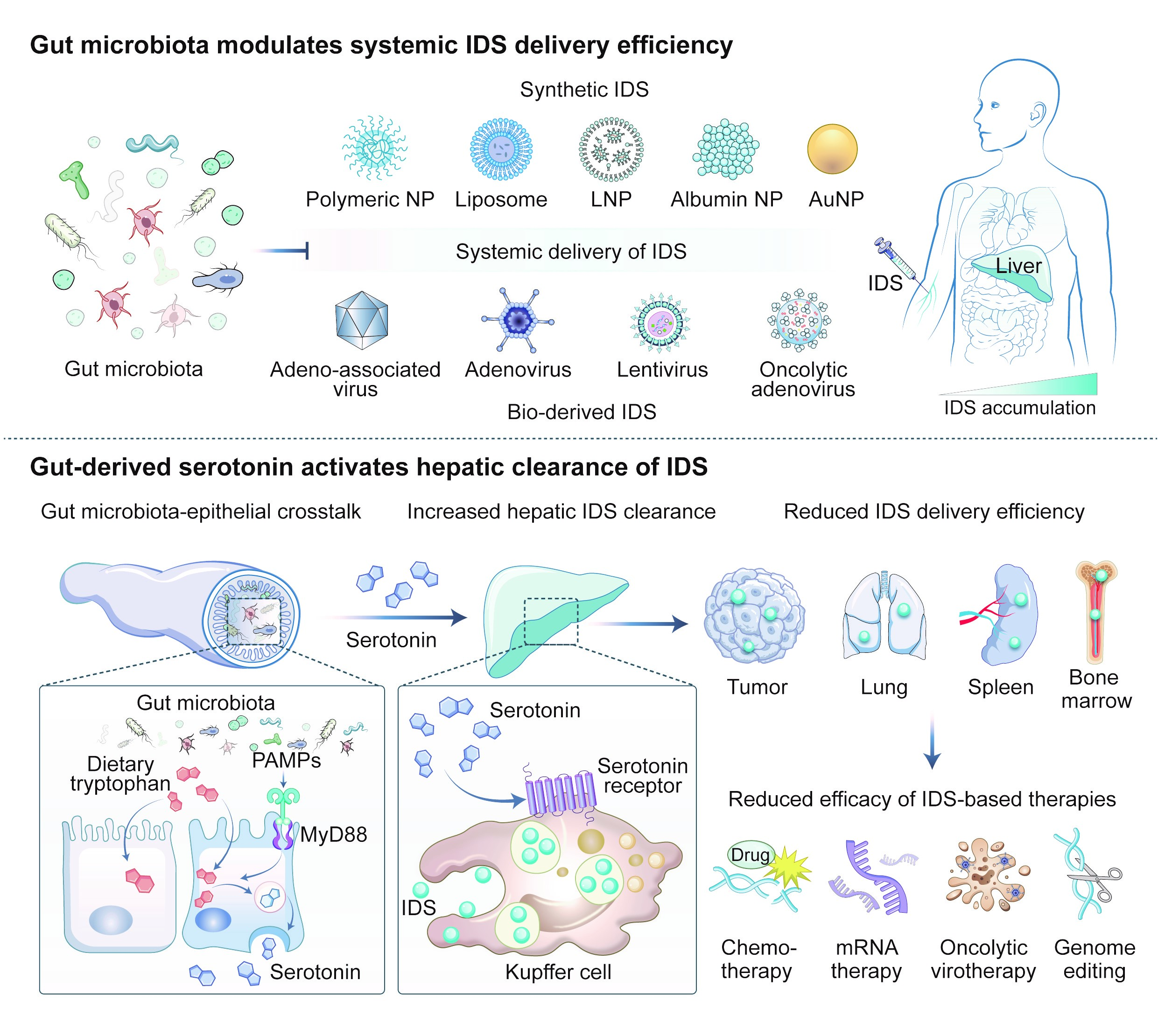
图 肠道共生菌通过刺激肠道血清素分泌维持肝脏对递送载体的清除活性
长期以来,科学家们普遍认为,大部分进入血液中的药物载体会被肝脏这个“中央处理站”清除掉。在国家自然科学基金项目(批准号:52025036、52495014、52522320、52273156、52473154)等资助下,中国科学技术大学王育才教授团队与合作者取得的研究发现颠覆了现有认知。
药物在体内的去留,其实由一个跨器官网络:“肠道—肝脏”共同调控。居住在我们肠道里的共生菌通过影响血清素的分泌,经由“门静脉”这条血管“高速路”,将信号直接传递至肝脏,远程“指挥”肝脏里的免疫细胞的功能状态,进而影响免疫细胞对药物载体的吞噬作用,并最终影响体内递送效率。
该研究的相关成果以“肠道共生菌驱动的血清素产生调节合成载体与病毒载体的体内递送(Commensal-driven serotonin production modulates in vivo delivery of synthetic and viral vectors)”为题,于2026年3月20日在线发表于《科学》(Science)杂志上。论文链接: https://www.science.org/doi/10.1126/science.adu7686。
药物递送载体通过调控药物在体内的时空分布与释放行为,减少副作用并增强疗效,已成为生物医药领域的核心底层技术。药物载体在血液循环中的分布特征及其清除行为是决定其体内递送效率的核心环节。然而,长期以来,对药物载体体内过程的认知主要局限于“肝脏单器官主导清除”的简化模型,缺乏对其在整体生理系统中动态转运与调控机制的系统理解,导致结构设计与体内行为之间缺乏可预测映射关系,限制了递送载体从经验优化向理性设计的转变。
为突破“肝脏单器官主导清除”的传统认知局限,研究团队基于活体显微成像技术建立了单细胞尺度的体内定量分析方法,从多器官协同视角系统解析了递送载体的循环分布与清除机制。研究首次发现了递送载体的体内行为并非由肝脏单一器官决定,而是受跨器官网络共同调控。研究揭示了一条“肠道—肝脏”跨器官调控通路机制:肠道共生菌通过调控血清素生成,经门静脉作用于肝脏巨噬细胞,增强其对递送载体的清除能力。基于这一多器官调控机制,通过干预代谢或饮食,可在不改变递送材料结构的前提下,延长药物载体循环时间,将体内递送效率提高约2–3倍,并显著增强肿瘤治疗(提升抗肿瘤疗效5倍以上)、基因编辑(提升基因编辑效率10–15倍)及mRNA治疗(提升核酸药物表达效率10倍以上)效果。该研究将递送机制从“单器官被动清除”拓展为“多器官主动调控”,为建立可预测、可调控的高效药物递送系统提供了新的设计范式。