 打印
打印
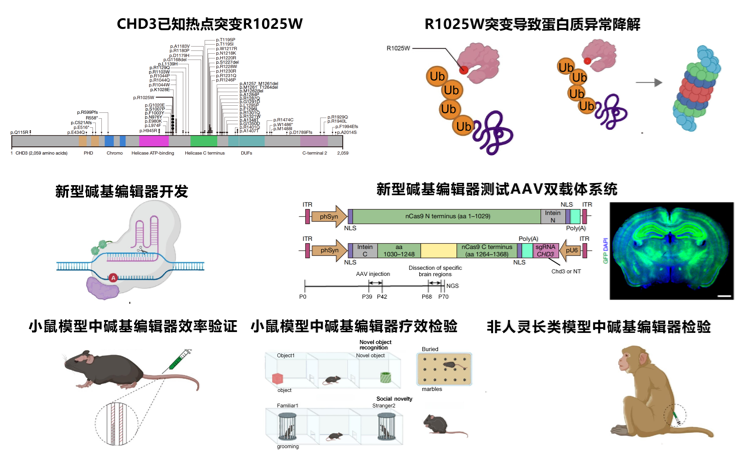
图 基因编辑治疗神经发育性疾病SNIBCPS
在国家自然科学基金项目(批准号:82430046、82001211、82360226、82471501)等资助下,上海交通大学医学院松江研究院仇子龙教授团队、复旦大学脑科学转化研究院程田林研究员团队、上海交通大学医学院附属新华医院李斐教授团队和杨侃副研究员团队合作,在神经发育性疾病基因治疗研究方面取得进展。研究成果以“在体碱基编辑Chd3基因改善小鼠行为异常(In vivo base editing of Chd3 rescues behavioural abnormalities in mice)”为题,于2026年2月18日在线发表于《自然》(Nature)杂志。论文链接:https://www.nature.com/articles/s41586-026-10113-6。
Snijders Blok-Campeau 综合征(SNIBCPS)是由CHD3基因突变引发的典型神经发育性疾病,导致儿童出现自闭症特征、全面发育迟缓、语言障碍、智力障碍及肌张力低下等一系列问题。目前由于SNIBCPS病因复杂、缺乏准确修复碱基突变的手段,尚缺乏针对性治疗方案。
研究团队针对SNIBCPS在CHD3基因的临床高频致病突变(p.R1025W),首先构建复刻患者核心症状的人源化突变小鼠模型,证实该突变会导致CHD3蛋白水平显著下降,干扰神经发育相关基因的表达,导致社交回避、认知迟钝、运动不协调等行为异常。随后,团队开发了新型腺嘌呤碱基编辑器TeABE(TadA-embedded adenine base editor,TeABE),可在不切断DNA双链的前提下,将突变的A-T碱基对修复为正常G-C碱基对,解决了传统基因编辑易造成基因组紊乱的难题。利用尾静脉注射双腺相关病毒(Dual AAV)递送系统,成功跨越血脑屏障,在小鼠大脑关键脑区实现突变位点准确修复。研究发现,碱基编辑不仅显著恢复了CHD3蛋白的表达及全脑转录组稳态,更在功能水平上显著改善小鼠的社交回避、认知迟钝、运动不协调等行为异常。为验证安全性,团队利用GUIDE-seq技术全基因组排查,发现TeABE在人类细胞中脱靶编辑率低于1%,小鼠脑中未检测到明显的脱靶效应。在非人灵长类猕猴模型中,鞘内注射AAV9-TeABE实现了编辑器高效表达与碱基编辑活性,验证了技术的跨物种应用可行性(图)。
该研究证实了出生后脑内的在体单碱基精准编辑可恢复蛋白功能、逆转神经发育缺陷,为SNIBCPS等单基因神经发育疾病提供了全新靶向治疗路径,也为其他单基因遗传病精准治疗提供了研究范式。