 打印
打印
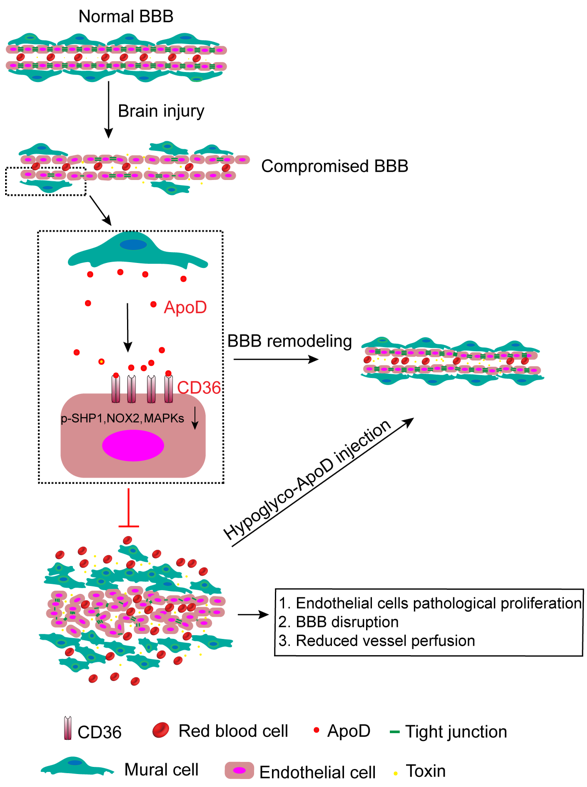
图 ApoD—脑梗死后神经血管炎症内源性刹车系统
在国家自然科学基金项目(批准号:82090040、81830039、82271351)等资助下,陆军军医大学第二附属医院杨清武教授、李芳菲教授、谢琦教授团队在中枢神经系统损伤后血脑屏障修复机制研究方面取得新进展。研究成果以“ApoD作为CD36全新抑制性配体,促进脑梗死后血脑屏障的修复(Apolipoprotein D, a Novel Ligand for CD36, Is Essential for Blood-Brain Barrier Integrity)”为题,于2026年2月6日在线发表于《循环》(Circulation)杂志。论文链接:https://doi.org/10.1161/CIRCULATIONAHA. 125.077356。
缺血性脑卒中是导致死亡和致残的主要原因之一,其发病机制复杂。血脑屏障的完整性对于维持脑内微环境稳态至关重要,而血脑屏障的破坏被认为是卒中后继发性脑损伤的核心病理环节。虽然血管壁细胞与内皮细胞间的通讯被认为是维持血脑屏障稳态的重要因素,但其具体的分子机制及病理调控网络仍未完全阐明,限制了针对血脑屏障修复的靶向药物研发。
研究发现血管壁细胞来源的载脂蛋白D(ApoD)通过抑制性结合内皮细胞表面的CD36从而促进血脑屏障修复的血管保护新机制。进一步研究表明,缺血性脑卒中发生后,ApoD通过直接结合内皮细胞表面的CD36,发挥特异性的“双重抑制”作用:一方面,它与CD36的经典激活配体——长链脂肪酸竞争结合胞外结构域;另一方面,它直接阻断CD36下游的病理性信号转导。这种分子阻断效应有效遏制了缺血诱发的病理性内皮细胞过度增殖,从而维持微血管结构稳定,显著减轻脑水肿并缩小梗死体积。进一步,团队深入解析了ApoD的结构-功能关系,发现其糖基化修饰状态是调控CD36抑制效能的关键“分子开关”。研究证实,相比完全糖基化的天然形式,低糖基化ApoD对CD36展现出更强的结合亲和力。这种构象优化后的ApoD能更高效地执行抑制功能,在限制血脑屏障渗漏、促进神经功能恢复及提高长期生存率方面具有更卓越的治疗潜能(图)。
该研究揭示了“壁细胞ApoD—内皮细胞CD36”旁分泌轴在神经血管单元重塑中的核心作用。为脑卒中、阿尔茨海默病、多发性硬化等伴有血脑屏障损伤的中枢神经系统疾病提供了基于“受体-配体”互作的精准治疗新策略,也提示低糖基化ApoD作为功能优化的蛋白药物具有广阔的转化前景。