 打印
打印
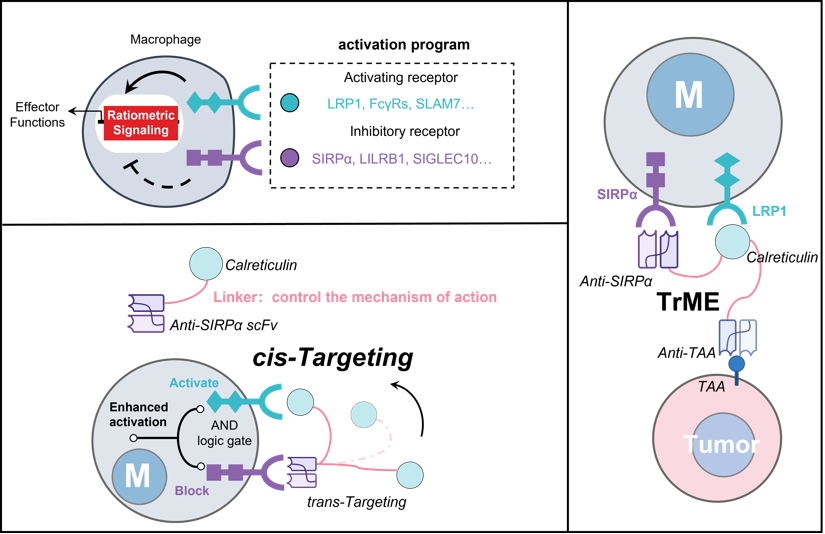
图 逻辑门控三特异性巨噬细胞衔接器的设计策略及作用机制示意图
在国家自然科学基金项目(批准号:82425056、82350125、82173763、82303810)等资助下,山东大学姜新义教授和赵坤教授、国家癌症中心/中国医学科学院肿瘤医院邢念增教授、山东大学赵法宝副研究员、南京大学张峻峰教授、山东大学荆卫强教授等开展合作,在逻辑门控免疫细胞衔接器治疗实体瘤研究方面取得进展。研究成果以 “逻辑门控三特异性衔接器增强巨噬细胞对实体瘤细胞的杀伤作用(A logic-gated trispecific engager enhances macrophage killing of cancer cells in solid tumors)” 为题,于2026年3月13日在线发表在《自然·生物技术》(Nature Biotechnology)杂志。论文链接https://www.nature.com/articles/s41587-026-03057-9。
免疫细胞衔接器是一类能够桥接免疫细胞与肿瘤细胞并诱导免疫细胞精准杀伤肿瘤的新型免疫治疗分子。近年来,该类药物在血液系统肿瘤治疗中取得显著进展,但在实体瘤中的应用仍面临挑战,其中肿瘤微环境的免疫抑制效应以及免疫信号整合不足是限制疗效的重要因素。巨噬细胞是实体瘤微环境中高度富集的重要免疫细胞,其吞噬功能依赖于促吞噬信号与抗吞噬信号之间的动态平衡。然而,现有治疗策略通常仅增强促吞噬信号或阻断抗吞噬信号,难以在单一细胞内实现多种信号的协同调控。
针对这一问题,研究团队设计并构建了一种逻辑门控三特异性巨噬细胞衔接器(Trispecific Macrophage Engager,TrME)。该分子基于计算辅助的顺式靶向策略,采用柔性连接子将单价低密度脂蛋白受体相关蛋白1(LRP1)激动剂钙网蛋白、抗调节蛋白α(SIRPα)单链抗体以及肿瘤相关抗原(TAA)靶向结构域串联,通过构建“激活+阻断”的“与”逻辑门控(AND logic gate),实现巨噬细胞表面促吞噬信号和抗吞噬信号效应的同步调节。研究结果表明,TrME能够增强肿瘤相关巨噬细胞吞噬能力,并促进其促炎性表型转化,形成免疫激活型肿瘤微环境。结合mRNA-脂质纳米颗粒递送系统,TrME可在多种实体瘤模型中实现体内表达,显著抑制肿瘤生长,同时未观察到明显的系统性毒性(图)。
该研究提出了一种基于顺式逻辑门控的免疫细胞衔接器设计策略,为多特异性免疫治疗分子的工程化设计提供了思路,也为克服实体瘤免疫抑制性微环境、提升免疫治疗效果提供了策略。