 打印
打印
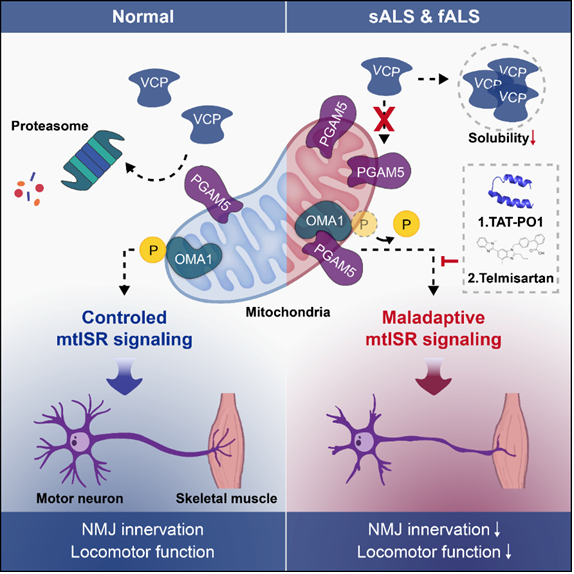
图1 VCP-PGAM5-mtISR轴在ALS中的病理机制及靶向干预策略
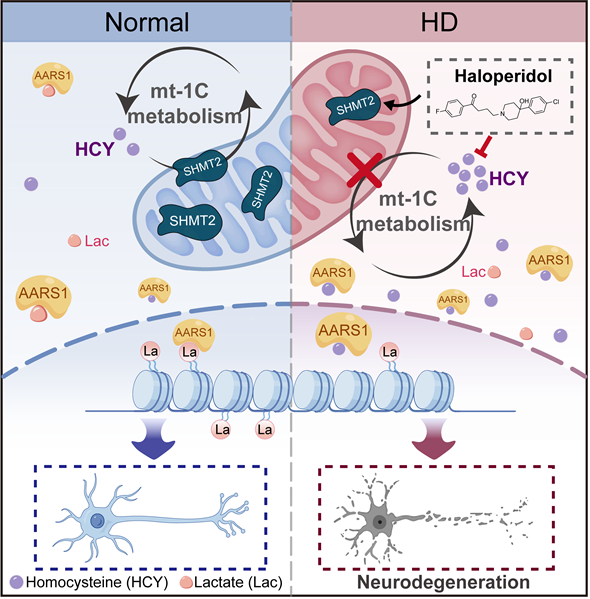
图2 SHMT2-HCY-组蛋白乳酸化轴在HD中的病理机制及靶向干预策略
在国家自然科学基金项目(批准号:U23A20429、82371260、82325015)等资助下,南京医科大学郭兴教授团队与国内学者合作研究,在神经退行性疾病发病机制及靶向治疗领域取得系列进展。其中,南京医科大学郭兴教授、刘妍教授和陈盼盼副教授团队在肌萎缩侧索硬化症(Amyotrophic Lateral Sclerosis,ALS)发病机制及靶向治疗研究方面取得新进展,研究成果以“靶向PGAM5驱动的线粒体整合应激反应延缓肌萎缩侧索硬化症不同亚型进展(Targeting PGAM5-driven mitochondrial integrated stress response slows ALS progression across subtypes)”为题,于2026年3月11日在线发表于《神经元》(Neuron)杂志,论文链接:https://www.cell.com/neuron/fulltext/S0896-6273(26)00086-3。同时,南京医科大学郭兴教授、刘妍教授与河北医科大学宋学琴教授团队合作,在亨廷顿病(Huntington's Disease,HD)发病机制研究方面取得新进展,研究成果以“SHMT2缺乏通过同型半胱氨酸介导的组蛋白乳酸化抑制破坏亨廷顿病模型中的转录调控(SHMT2 deficiency disrupts transcriptional regulation through homocysteine-mediated suppression of histone lactylation in Huntington's Disease models)”为题,于2026年3月10日在线发表于《临床研究杂志》(Journal of Clinical Investigation)杂志,论文链接:https://www.jci.org/articles/view/196094。
神经退行性疾病是一类以脑和脊髓特定神经元进行性退变为核心病理特征的疾病,最终导致患者运动、认知等功能障碍。其中,ALS及HD的部分致病基因虽已被发现,但引起神经元变性死亡的分子机制尚未阐明,目前仍缺乏有效控制疾病进展的干预措施,亟需深入解析其机制并开发新型干预策略。
线粒体不仅是能量代谢的核心执行单元,更是感知细胞状态、整合多源信号的信息处理中心。在神经退行性疾病发生发展过程中,线粒体相关酶功能异常可能参与神经元变性死亡。研究团队发现,线粒体磷酸甘油酸变位酶5(PGAM5)是含缬酪肽蛋白质(VCP)的底物,且在散发性ALS患者脊髓、散发性和家族性ALS患者来源iPSC分化的人脊髓类器官及ALS小鼠模型中均显著上调,PGAM5可通过对线粒体内膜金属蛋白酶(Overlapping with the m-AAA protease 1 homolog,OMA1)的去磷酸化激活线粒体整合应激反应(mtISR),介导线粒体-细胞核通讯异常并引发运动功能障碍;而采用多肽TAT‑PO1阻断PGAM5‑OMA1相互作用,或使用替米沙坦(telmisartan)抑制PGAM5活性,均可抑制mtISR异常激活、改善ALS相关神经病理及运动功能障碍(图1)。
此外,研究团队在HD患者来源iPSC分化的人纹状体类器官及YAC128转基因小鼠模型中,发现线粒体一碳代谢关键酶SHMT2下调导致同型半胱氨酸(homocysteine,HCY)异常升高,后者通过竞争性结合丙氨酰-tRNA合成酶1(alanyl-tRNA synthetase 1,AARS1)抑制组蛋白乳酸化修饰,造成代谢-表观遗传失调,进而损害中型多棘神经元结构及功能完整性,最终导致神经元死亡;进一步研究发现HD症状管理药物氟哌啶醇(haloperidol)可通过上调SHMT2、降低HCY水平并恢复组蛋白乳酸化,从而改善神经元结构与功能(图2)。
系列研究从线粒体-细胞核通讯角度深化了对神经退行性疾病病理机制的理解,为早期减缓ALS及HD疾病进程、开发疾病治疗新靶点提供了理论依据,也为老药新用及临床转化研究开辟了新方向。