 打印
打印
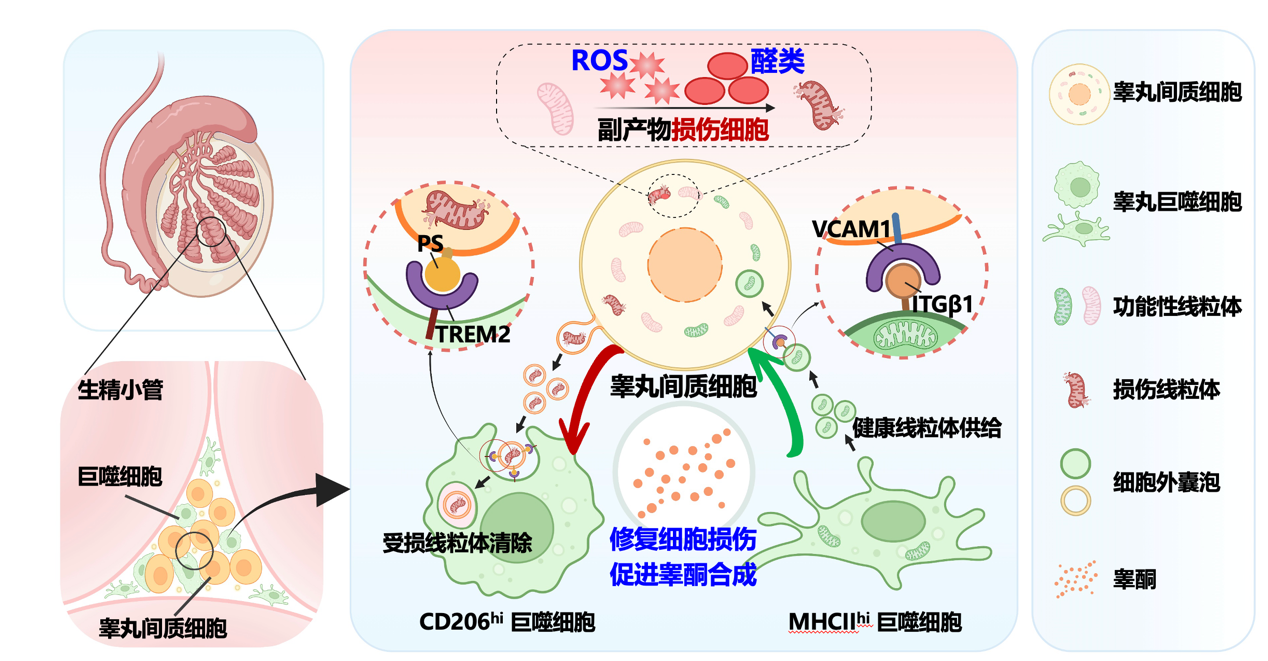
图 双向线粒体转移维持生精微环境稳态的作用机制
在国家自然科学基金项目(批准号:82430050、82371611、82371609)等资助下,中山大学项鹏教授、肖海鹏教授、邓春华教授和陈莉莉教授团队在双向线粒体转移网络维持生精微环境稳态及睾酮合成的研究方面取得进展。相关研究成果以“细胞外囊泡介导的线粒体双向转移网络维持睾酮合成的新机制(An extracellular vesicle-mediated mitochondrial transfer network critical for testosterone synthesis)”为题,于2026年2月27日在线发表于《自然-细胞生物学》(Nature Cell Biology)杂志上。论文链接为:https://www.nature.com/articles/s41556-026-01896-x。
睾丸间质细胞(Leydig Cells,LCs)合成了体内超过95%的睾酮及多种蛋白因子,是生精微环境的重要组分,对于维持男性生殖功能与全身生理稳态至关重要。线粒体在LCs的功能发挥中扮演核心作用,但LCs合成睾酮过程产生的活性氧、醛类会损伤线粒体。LCs如何维持线粒体稳态以保障其功能完整性尚有待阐明。
为探究这一机制,研究团队通过遗传学模型和示踪技术首次发现,LCs与睾丸巨噬细胞之间通过胞外囊泡形成“双向线粒体转移网络”。 在睾酮合成活跃时,LCs可排出包裹受损线粒体的胞外囊泡,由CD206hi巨噬细胞作为“清道夫”,通过TREM2受体高效识别并清除;同时,MHCIIhi巨噬细胞作为“捐赠者”,将包裹健康线粒体的胞外囊泡精准递送至LCs,经LCs表面VCAM1识别并内吞,从而帮助其重建线粒体网络。阻断该双向转移过程会导致睾酮合成障碍,引发睾丸萎缩、生精障碍、生育力降低、肌肉功能衰退。研究还发现老年小鼠中线粒体转移效率显著下降,其可能为年龄相关睾丸功能衰退的重要原因(图)。
该研究描绘了睾丸内精密的双向线粒体转移网络,打破了以往对细胞间线粒体转运的固有认知,揭示了间质细胞与巨噬细胞亚群之间的协同互作模式——通过“弃旧换新”的动态调控,解决了间质细胞因高代谢负荷导致的线粒体损伤难题,保障了睾酮持续稳定合成。研究结果为治疗睾酮合成障碍相关疾病,特别是衰老相关的性腺功能减退提供了思路。