 打印
打印
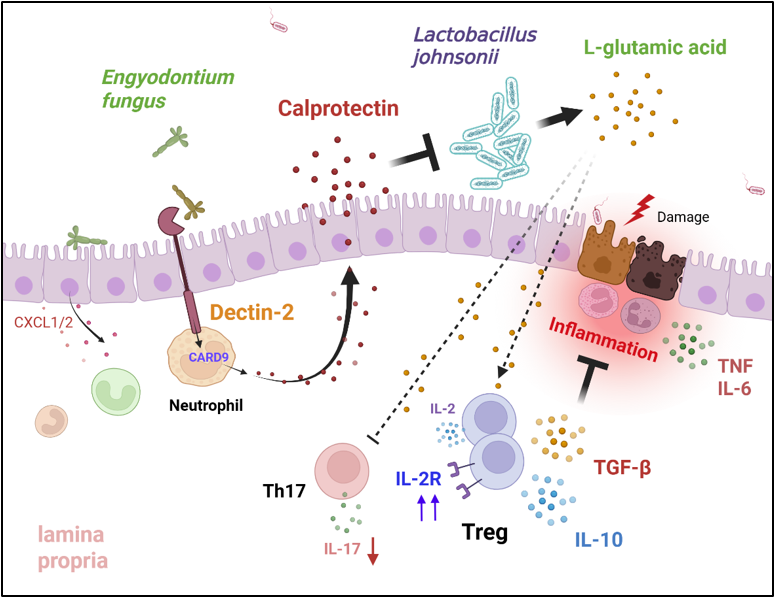
图 肠道侧齿霉菌通过激活固有免疫系统调控肠黏膜炎症
在国家自然科学基金项目(批准号:82370540、82070564、82403250)等资助下 ,中山大学附属第一医院唐策研究员、黄婵燕副主任医师、冯瑞副主任医师、陈旻湖教授等团队在共生真菌通过固有免疫受体调控肠道炎症机制方面取得进展。相关研究成果以“结肠侧齿霉菌通过激发中性粒细胞抗菌活性抑制约氏乳杆菌及其代谢产物谷氨酸以抑制调节性T细胞(Colonic Engyodontium fungus triggers neutrophil antimicrobial activity to suppress Lactobacillus johnsonii-derived glutamic acid-maintained Tregs)”为题,于2026年3月2日在线发表于《临床研究杂志》(Journal of Clinical Investigation)上 。论文链接:https://doi.org/10.1172/JCI196788。
炎症性肠病(inflammatory bowel disease, IBD)包括克罗恩病(CD)和溃疡性结肠炎(UC),是由于遗传、微生物及免疫因素相互作用导致的慢性肠道炎症。虽然肠道微生物群在IBD的发病中起着关键作用,但目前的研究大多聚焦于细菌,共生真菌在肠道稳态中的功能因分离培养困难而仍不清晰。研究表明,模式识别受体在感应肠道微生物并维持免疫稳态中至关重要。然而,特定的肠道共生真菌如何通过宿主免疫受体调节细菌群落并进而影响调节性T细胞(Treg)介导的免疫稳态,其具体机制尚不明确。
为了探究这一关键问题,研究团队利用Dectin-2–Fc融合蛋白纯化技术,首次从肠道中分离并鉴定了一种关键共生真菌侧齿霉菌(Engyodontium sp.)。研究发现,该真菌通过激活中性粒细胞表面的Dectin-2–CARD9信号轴,诱导抗菌肽钙卫蛋白(Calprotectin, S100A8/A9)的大量产生。进一步研究证实,钙卫蛋白通过其抗菌活性选择性抑制肠道益生菌约氏乳杆菌(Lactobacillus johnsonii)WXY菌株的定植。该乳杆菌可利用谷氨酰胺酶(glsA)产生代谢产物L-谷氨酸,后者通过增强白介素2受体CD25信号促进Treg细胞的扩增与功能。Engyodontium对约氏乳杆菌的抑制导致肠道 L-谷氨酸水平下降,进而削弱了Treg细胞介导的免疫保护,显著加剧了结肠炎进展。临床样本分析显示,IBD患者体内Engyodontium丰度显著升高,且与约氏乳杆菌及谷氨酸水平呈负相关(图)。
该研究揭示了肠道内“真菌–中性粒细胞–细菌–代谢产物”这一跨界调控轴在IBD发病中的致病机制,拓展了C型凝集素受体在感应共生真菌并重构微生态功能方面的认知。该研究提出了通过干预特定真菌及其下游信号轴来恢复肠道稳态的新策略,为IBD的精准治疗及营养干预提供了新途径。