 打印
打印
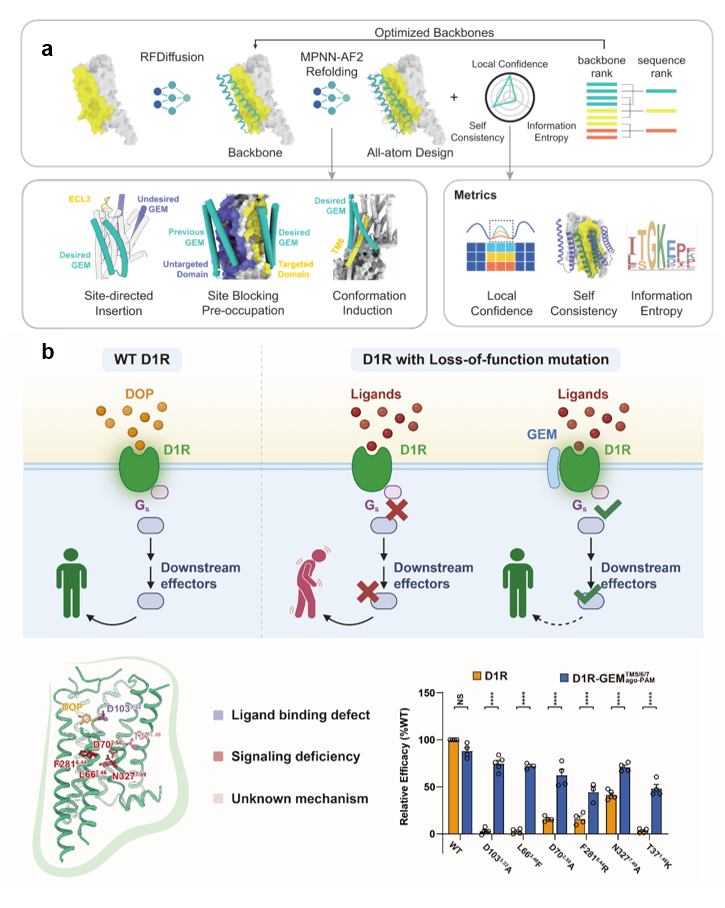
图 G蛋白偶联受体外骨骼蛋白(GEM)的AI从头设计和失活突变受体功能修复
在国家自然科学基金项目(批准号:92353303、32430051、32141004、62202426)等资助下,浙江大学基础医学院张岩团队于2026年2月17日在《Nature》(自然)期刊上发表题为“De novo Design of GPCR Exoframe Modulators”的研究论文,论文链接为https://www.nature.com/articles/s41586-025-09957-1。该研究创建了膜蛋白功能设计的新范式,通过深度学习从头设计了靶向G蛋白偶联受体(GPCR)跨膜结构域的外骨骼调节剂(GEM),实现了对受体功能的多样化精准调控,为治疗GPCR功能缺失突变相关疾病提供了全新的治疗策略。
G蛋白偶联受体是人体内最大的膜蛋白家族,也是最重要的药物靶点。传统药物主要通过结合内源性配体的“正构位点”发挥作用。然而,这种作用方式常因位点保守性导致选择性较差、副作用较大,且难以修复由功能缺失突变引起的受体功能障碍。自然界中存在一类跨膜蛋白,如受体活性调节蛋白,能够通过跨膜相互作用调节GPCR功能,这为开发新型调节剂提供了灵感。然而,针对GPCR跨膜域进行功能导向的蛋白质从头设计,仍极具挑战。
上述团队建立了一套基于深度学习的探针算法及一个“类幻觉”(hallucination-like)蛋白质从头设计流程(图a)。利用AlphaFold2-multimer进行高通量结构预测,结合RFDiffusion和ProteinMPNN等先进算法,定位了潜在的跨膜调控位点,提出了三种“结构提示”(Structural Prompting)策略——位点导向插入、位点阻断预占和构象诱导。通过这些策略,研究人员能够在设计过程中通过施加结构约束,引导生成具有特定结合模式和功能的跨膜蛋白。
该团队以多巴胺D1受体(D1R)为模型,设计并验证了四种具有不同功能的GEMs:锚定型(Anchor)、偏向性别构调节剂(BAM)、负向别构调节剂(NAM)和激动-正向别构调节剂(ago-PAM)。结构生物学研究与功能实验表明,这些从头设计的GEM能以极高的精度靶向D1R的跨膜结构域。其中,BAM型GEM展示了通过靶向特定界面实现信号通路选择性(偏向性信号)的潜力;NAM型GEM则能有效锁定受体失活构象; ago-PAM型GEM可通过稳固受体的激活构象(TM6外移)恢复多种D1R功能缺失突变体(包括与帕金森综合征相关的突变)的信号转导活性(图b)。
该研究证明了深度学习在膜蛋白功能化设计中的可行性,并提出了一种以跨膜蛋白为核心的药物模态。作为一种可编程调控工具,GEM能够对受体功能进行调控和修复,为GPCR别构调节和结构生物学研究提供了工具。