 打印
打印
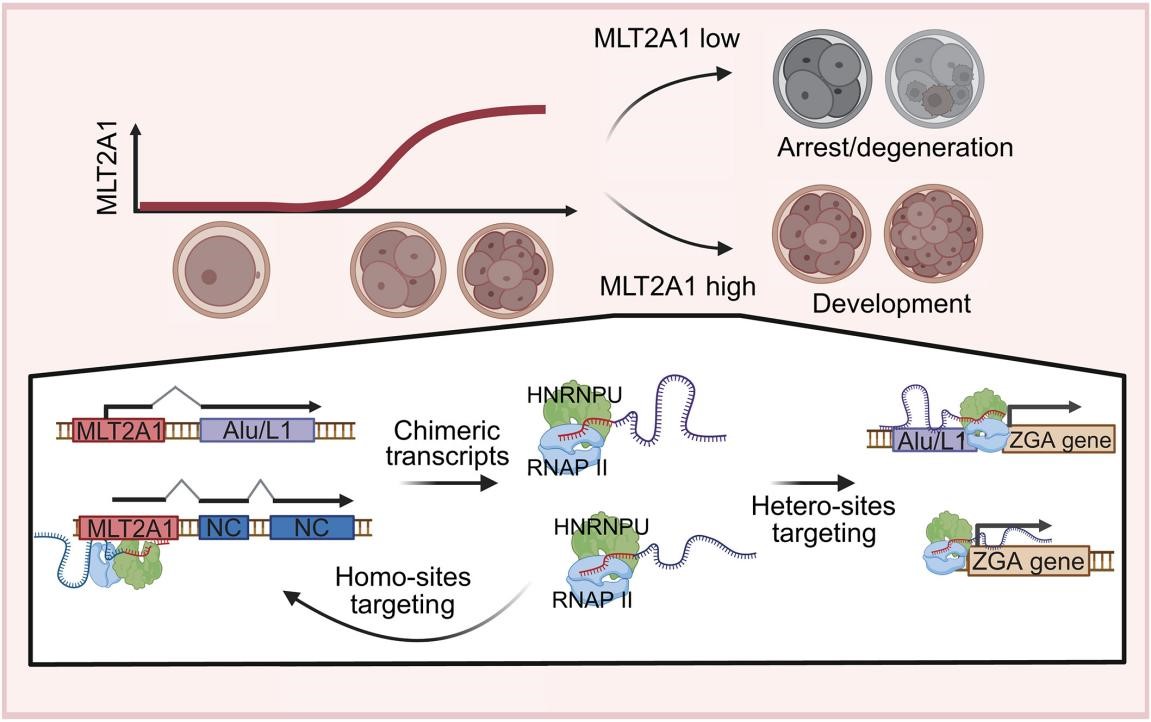
图 MLT2A1通过合成异源嵌合RNA增强人类ZGA
在国家自然科学基金项目(批准号:32470783、82394424、32488101)等资助下,浙江大学梁洪青研究员、张丹教授团队联合同济大学高绍荣教授、浙江大学爱丁堡大学联合学院刘琬璐研究员团队,在内源性逆转录病毒调控人类胚胎发育研究领域取得进展。相关研究成果以“内源性逆转录病毒形成嵌合转录本调控人类早期胚胎发育(Endogenous retroviruses synthesize heterologous chimeric RNAs to reinforce human early embryo development)”为题,于2026年1月22日在线发表于《科学》(Science)杂志上。论文链接:https://www.science.org/doi/10.1126/science.adv5257。
人类胚胎常在受精后至着床前的关键发育节点停滞,导致不孕和妊娠丢失。合子基因组激活(ZGA)作为受精后胚胎启动自身基因组转录的核心事件,是胚胎实现自主发育的决定性转折,其异常是导致早期发育阻滞的主要原因之一。然而,ZGA失败导致妊娠丢失的机制仍不明确。内源性逆转录病毒(Endogenous Retroviruses, ERV)是一类特殊的逆转座序列,在基因组中拥有大量序列相似的拷贝。特定ERV亚家族在ZGA阶段特异性激活,转录产生高丰度的RNA,但其在胚胎发育中的功能未得到明确阐释。
针对发育生物学和生殖医学的这些难题,研究团队发现,停滞在8-细胞合子基因组激活时期的人类胚胎中,ERV亚家族MLT2A1表达显著下调。在胚胎中敲低MLT2A1,8-细胞期的发育比例从47%骤降至16%,且ZGA关键基因表达大幅下降。团队进一步利用纳米孔长读长测序技术,发现MLT2A1亚家族的不同拷贝可以与其下游序列形成嵌合转录本,其中超过70%的嵌合转录本融合了其他亚家族的逆转座子(如LINE1、Alu)序列,从而极大地扩展了MLT2A1 RNA的序列复杂性。进一步的生化实验表明,MLT2A1 RNA一方面利用其多样的融合序列广泛结合ZGA 基因及其调控序列,另一方面通过其保守序列特异性结合核蛋白HNRNPU招募RNA聚合酶II,从而帮助结合位点附近的ZGA基因激活。同时,研究还发现MLT2A1的不同拷贝可以相互协同激活,形成一个自我放大的协同网络,共同参与全局性ZGA基因的调控(图)。
该研究系统地阐明了内源逆转录病毒转录本通过“序列融合-靶向扩展-协同放大”机制调控人类早期胚胎发育,深化了对人类生命起始阶段发育调控机制的理解,也为改善辅助生殖技术提供了新思路。
