南医大姚兵团队揭示肿瘤缺氧微环境驱动铜死亡抵抗的机制
近日,基础医学院姚兵副教授团队在《细胞•癌症》(Cancer Cell)发表题为 《HIF-1α驱动肿瘤铜死亡抵抗》(Hypoxia inducible factor-1 drives cancer resistance to cuproptosis)的研究论文。该研究揭示了HIF-1α通过调控PDK1/3 - DLAT通路和MT2A表达抑制铜死亡的关键机制,提出HIF-1α抑制剂联合铜离子/铜载体作为实体肿瘤治疗新策略,并在多种原位肿瘤模型中获得良好疗效,为临床转化治疗提供了新的思路。

铜死亡作为新发现的细胞死亡方式,其特点是铜离子载体促进铜离子进入细胞,导致脂酰化蛋白的异常聚集、线粒体呼吸中铁硫簇蛋白的破坏以及蛋白质毒性相关的应激反应的发生,最终导致细胞死亡。铜死亡作为新近发现的细胞死亡方式,在肿瘤治疗中具有重大潜力。然而实体肿瘤对铜死亡相对抵抗,限制了其在肿瘤治疗中的应用。
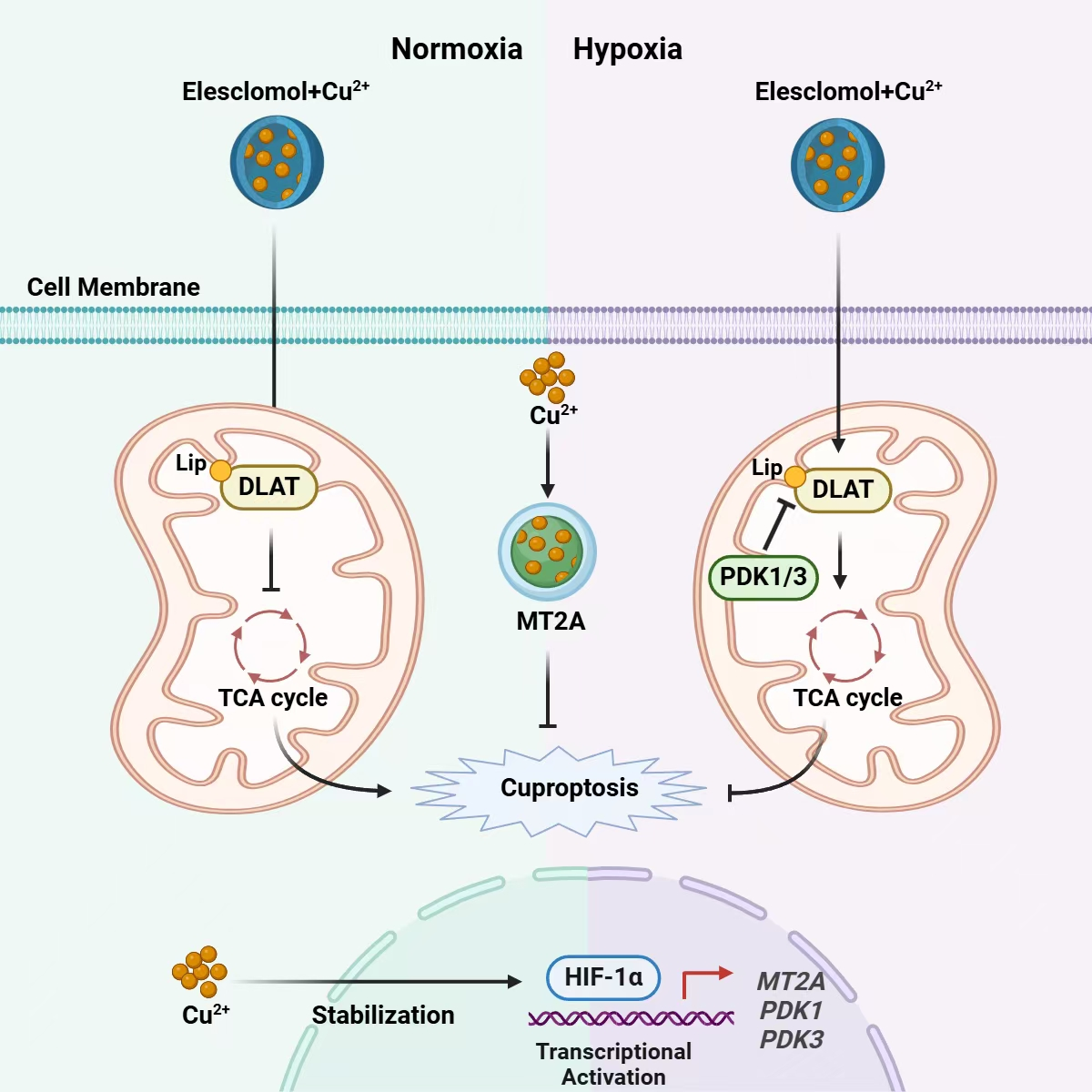
在本项研究中,姚兵团队发现HIF-1α诱导实体肿瘤细胞铜死亡抵抗的新机制。鉴定HIF-1α上调的MT2A是关键的、新的储铜蛋白,在细胞质中发挥储存游离铜离子的作用,为铜死亡领域研究提供了全新的思路;发现铜离子可稳定HIF-1α表达,通过上调PDK进而下调铜离子靶标DLAT,导致铜离子失去与Lip-DLAT结合的机会,进一步增强HIF-1α诱导铜死亡抵抗。发现HIF-1α抑制剂PX-478有效增敏实体肿瘤铜死亡,并在多种原位肿瘤模型中获得良好疗效,PX-478联合铜离子/铜载体策略不仅有效抑制小鼠肿瘤生长,并且小鼠脏器无任何损伤、体重无明显变化,说明PX-478联合铜离子/铜载体是一种低毒性且十分有效的肿瘤治疗新策略,为临床转化治疗提供了新的思路。
论文链接:https://linkinghub.elsevier.com/retrieve/pii/S1535610825000674
