|
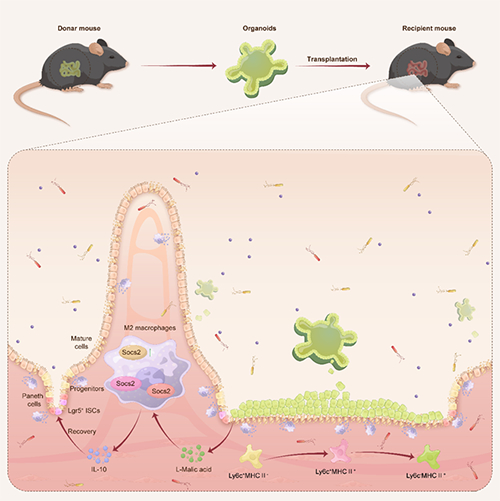 |
图 小肠类器官移植对肠缺血再灌注损伤的治疗作用
在国家自然科学基金项目(批准号:82172141)等资助下,南方医科大学刘克玄教授团队在小肠类器官治疗肠缺血再灌注损伤研究方面取得进展,研究成果以“类器官移植通过L-苹果酸介导的M2巨噬细胞极化减轻小鼠肠缺血再灌注损伤(Organoids transplantation attenuates intestinal ischemia/reperfusion injury in mice through L-Malic acid-mediated M2 macrophage polarization)”为题,于2023年10月25日在线发表于《自然·通讯》(Nature Communications)杂志。论文链接:https://doi.org/10.1038/s41467-023-42502-0。
肠缺血再灌注(Ischemia/Reperfusion,I/R)损伤是临床常见危重症之一,常见于创伤、感染、失血性休克、肠梗阻、急性肠系膜缺血、肠移植及体外循环手术等情况。肠I/R损伤发生后,黏膜上皮大量坏死,肠绒毛和隐窝脱落,继而出现肠屏障功能障碍及肠外并发症,最终死亡率高达50%-90%。目前虽已开发出一些方法来预防或治疗肠I/R损伤,但对于缺血后肠粘膜的修复仍有待研究。
该研究团队成功培养了小鼠小肠类器官并将其植入肠I/R后的受损肠粘膜组织,发现能显著提高小鼠的存活率,促进肠道干细胞的自我更新,并调节肠道I/R后的免疫微环境。通过代谢组学研究发现,L-苹果酸(L-Malic acid,MA)在器官组织衍生的条件培养基和移植小鼠盲肠内容物中均有高表达和富集,而体外循环心脏手术(包含肠I/R过程)患者术前粪便中的MA含量与术后肠损伤的程度存在明显的负相关,提示器官组织在移植过程中分泌MA。在此基础上,采用细胞因子信号转导抑制因子(Suppressor of cytokine signaling 2,SOCS2)基因敲除小鼠、巨噬细胞过继回输实验进一步探讨了MA在肠I/R损伤中的作用和保护机制,发现MA能以SOCS2依赖性方式诱导巨噬细胞M2极化,从而恢复IL-10水平,减轻肠I/R损伤(图)。
该研究揭示了移植的小肠类器官可通过促进肠干细胞自我更新和调节免疫微环境来缓解小鼠肠道I/R损伤,为临床治疗肠I/R损伤提供了新思路。