|
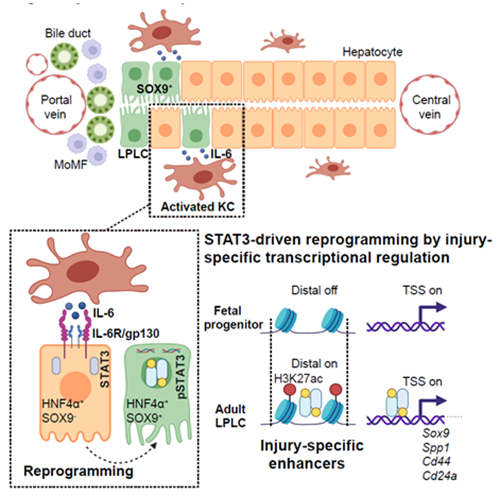 |
图 Kupffer细胞来源IL-6通过损伤特异增强子诱导肝细胞去分化机制
在国家自然科学基金项目(批准号:92168202、31930030、T2122018)等资助下,中国科学院分子细胞科学卓越创新中心惠利健研究员团队与中国科学院上海营养与健康研究所李虹和李亦学研究员团队合作,在炎症信号调控肝细胞去分化促进肝脏组织再生研究方面取得进展。研究成果以“枯否细胞来源的白细胞介素-6通过损伤特异增强子激活前体基因的方式被应用于肝细胞的去分化(Kupffer cell-derived IL-6 is repurposed for hepatocyte dedifferentiation via activating progenitor genes from injury-specific enhancers)”为题,于2023年2月13日在线发表于《细胞•干细胞》(Cell Stem Cell)杂志,论文链接:https://www.cell.com/cell-stem-cell/fulltext/S1934-5909(23)00009-7。
组织再生过程中新生细胞的来源主要有两种,一种来自于成体干细胞自我扩增并分化,另一种来自于原先存在的已分化的细胞。已分化的细胞可以通过去分化或者重编程的过程促进组织再生,该现象在多种组织器官中均有发现,例如:肺脏、肝脏、胰腺和小肠等。在肝脏的损伤再生修复过程中,成熟肝细胞发生去分化,重编程为Sox9+阳性类肝前体细胞(Liver progenitor-like cells, LPLCs),是肝脏组织再生的细胞重要来源之一。目前,肝细胞重编程的机制尚未完全清楚,阐明其具体机制对于开发诱导肝细胞去分化的药物来治疗肝脏损伤相关疾病具有重要的理论意义。
该研究团队利用单细胞测序技术解析肝细胞重编程过程中响应的损伤信号,发现免疫信号的激活与肝细胞重编程过程高度正相关;通过对肝脏不同种类免疫细胞的敲除,并结合不同巨噬细胞亚群敲除的小鼠模型,鉴定出Kupffer细胞是肝细胞重编程发生必要的巨噬细胞亚群;进一步对Kupffer细胞表达谱和Kupffer细胞特异分泌因子的筛选研究发现,IL-6通过结合肝细胞IL-6受体/gp130受体,可直接激活STAT3信号通路诱导肝细胞去分化,促进肝脏组织再生;利用结合位点分析法(ChIP-seq),证实STAT3作为转录因子结合在损伤特异的增强子上,促进了肝前体基因的表达。
本研究揭示了肝脏损伤后驻留巨噬细胞的炎症信号通过损伤特异的转录调控模式诱导肝细胞去分化、促进肝脏组织再生的分子机制(图),为开发诱导肝细胞去分化相关药物治疗肝脏疾病提供了潜在的作用靶点。