西电新闻网讯 近期学校计算机科学与技术学院高琳教授博士生胡宇轩和叶育森分别以第一单位在Nature子刊《Nature Communications》(IF=12.353, 中科院一区)及领域顶级期刊《Nucleic Acids Research》(IF=11.561,中科院一区)发表研究成果。


胡宇轩为论文“Optimal control nodes in disease-perturbed networks as targets for combination therapy”第一作者,高琳教授和宾夕法尼亚大学Tan Kai教授为共同通信作者,该论文提出了疾病联合治疗领域中一个崭新的问题:如何不局限于已有药物来开发新颖的联合治疗方案?对于人类常见复杂疾病,比如癌症,第一步治疗往往是手术切除实体肿瘤。然而,癌细胞很难被彻底清除。为了防止癌症复发,化疗、靶向治疗、免疫治疗及这些疗法的联合通常作为后续治疗方案。联合治疗通过对多种致病通路发挥作用,是对抗药物抗性和疾病异质性的有效策略。大多数联合治疗的开发侧重于确定现有药物的协同组合。然而,现有药物仅靶向蛋白质组的很小一部分。截至2016年,仅有667种人类蛋白质作为FDA批准药物的靶标,而人类共有超过2.1万个蛋白质编码基因。因此,大量基因及其组合仍未作为潜在的联合治疗靶标进行探索。
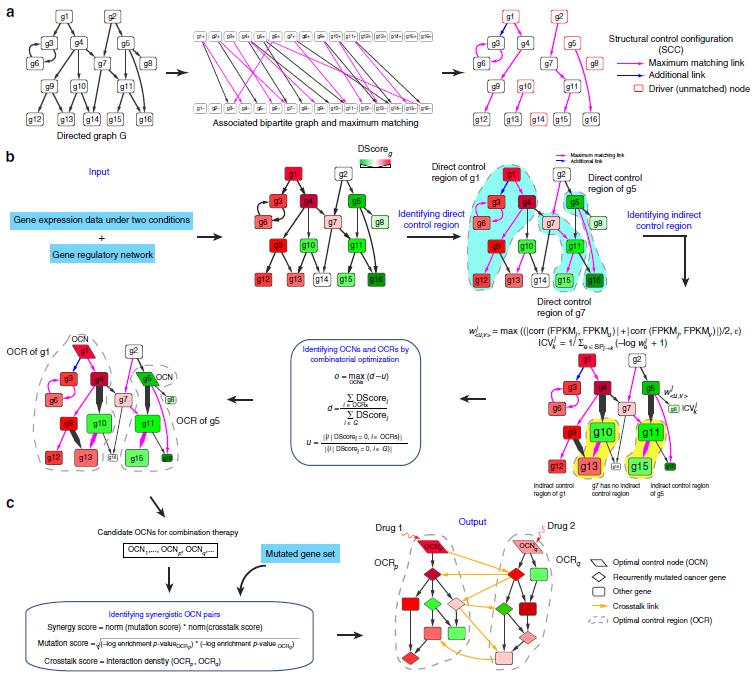
该论文通过使用基因表达作为网络可控性框架中的约束,开发了最优控制节点(OptiCon)算法,这是一个基于网络可控性理论,从基因网络中识别协同调控因子的创新性算法。该算法不需使用药物等先验信息,通过对网络模型上的组合优化问题求解,为疾病联合治疗提供新颖的候选靶标组合。研究者不仅通过计算层面对OptiCon预测结果进行评估,并使用CRISPR/Cas9基因编辑技术对结果准确性进行验证。
叶育森为论文“MSTD: an efficient method for detecting multi-scale topological domains from symmetric and asymmetric 3D genomic maps” 第一作者,高琳教授与中国科学院数学与系统科学研究院张世华研究员为共同通讯作者,该论文提出了一种有效的方法从3维基因组数据中检测多尺度的拓扑结构域。三维基因组学是人类基因组学发展的第三次浪潮,三维基因组结构异常与癌症等复杂疾病相关,本文正是在这样的背景下开展了三维基因组结构检测的算法研究。
哺乳动物的染色体折叠缠绕在细胞核中,并形成丰富的层次结构。从MB尺度的激活或者非激活的染色体子室 (compartments A/B),到百kb尺度的拓扑关联结构 (topologically associated domains, TADs) 或者子拓扑关联结构 (sub-TADs),再到更为精细的染色体环(chromatin loops)。这些结构已经被认为是影响基因调控、细胞内生物过程、细胞分化、进化等的重要因素。该研究旨在提出一个通用且高效的多尺度拓扑结构域识别方法MSTD,以从多种类型的三维基因组数据中鉴定多尺度的拓扑结构,其中包括顺式的(cis)和反式(trans)的交互结构。该方法不仅能够鉴定多尺度的拓扑关联结构(TADs),而且首次提出鉴定启动子锚定的交互结构域 (promoter-anchored interacting domains, PADs)和成对的拓扑关联交互结构域(pairwise topologically associating domains, PTADs)。
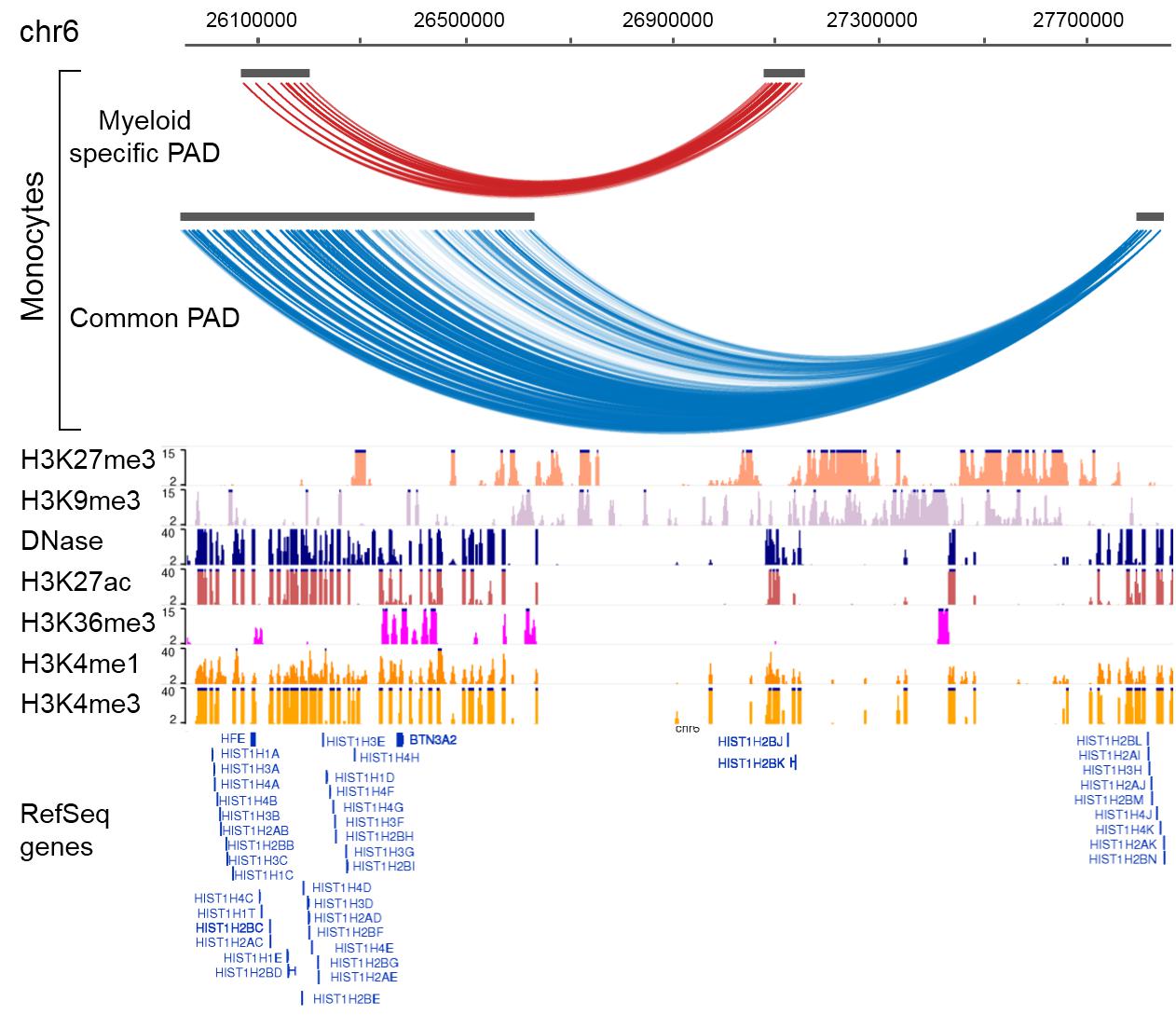
该方法被用于17个人类血液细胞promoter-capture Hi-C图谱。该研究指出PADs的类型可能通过边界区域表观因子的组合指定,并验证相似细胞之间的PADs更加保守,开创性的发现180个trans-interacting PAD。这些PADs被发现通过动态的染色质交互参与细胞特异的激活或者调控事件,为不同类型血液细胞的分析以及血液疾病的治疗提供依据。该方法同样适用从常见的Hi-C数据鉴定多尺度TADs以及PTADs,并在准确率和计算效率都表现明显的优越性。
以上2项研究成果得到了国家自然基金委重点项目(No.61532014),面上项目(No.61873198),科技部重点研发计划重点专项(No.2018YFC0910400)的资助。
相关链接:
论文链接:https://www.nature.com/articles/s41467-019-10215-y
论文链接:https://academic.oup.com/nar/advance-article/doi/10.1093/nar/gkz201/5426476